eTMF(전자 시험 마스터 파일) 시장 규모 및 추세 예측 – 2025년부터 2032년까지
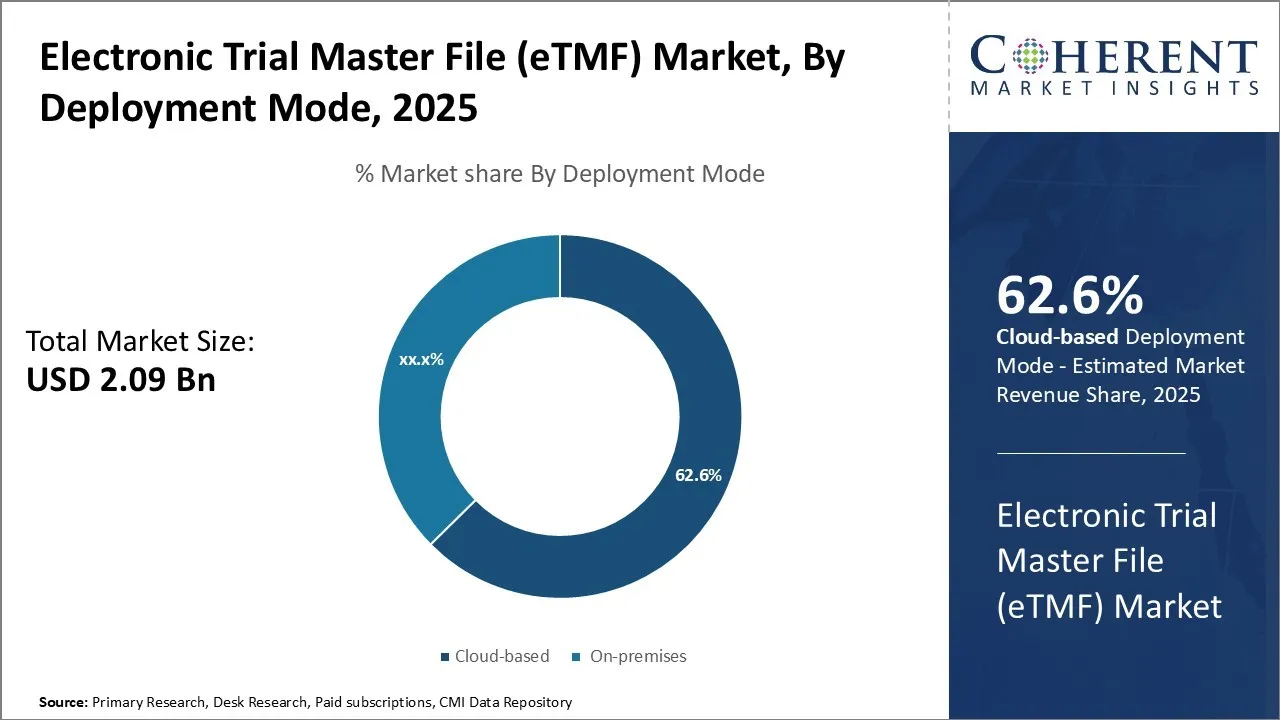
전자 시험판 마스터 파일(eTMF) 시장은 2025년에 미화 20억 9000만 달러로 평가되고 2032년에 미화 48억 1000만 달러에 도달하여 2025년부터 2025년까지 연평균 성장률(CAGR) 12.6%을 보일 것으로 예상됩니다. 2032.
이 보고서에 대해 자세히 알아보세요, 무료 샘플 다운로드
eTMF(전자 시험판 마스터 파일) 시장의 주요 시사점
- 배포 방식에 따라 클라우드 기반 부문은 2025년 시장 점유율 62. 6%를 차지할 것으로 예상됩니다.
- 기능별로 보면 문서 관리 부문은 2025년 40. 8%로 가장 높은 시장 점유율을 차지할 것으로 예상됩니다.
- 최종 사용자 측면에서 제약회사 부문은 2025년에 49%라는 가장 높은 시장 점유율을 차지할 것으로 예상됩니다.
- 북미는 eTMF(전자 시험판 마스터 파일) 시장에서 여전히 지배적인 위치를 유지하고 있으며 2025년에는 글로벌 시장 점유율의 35. 9%를 차지할 것으로 추정됩니다.
시장 개요
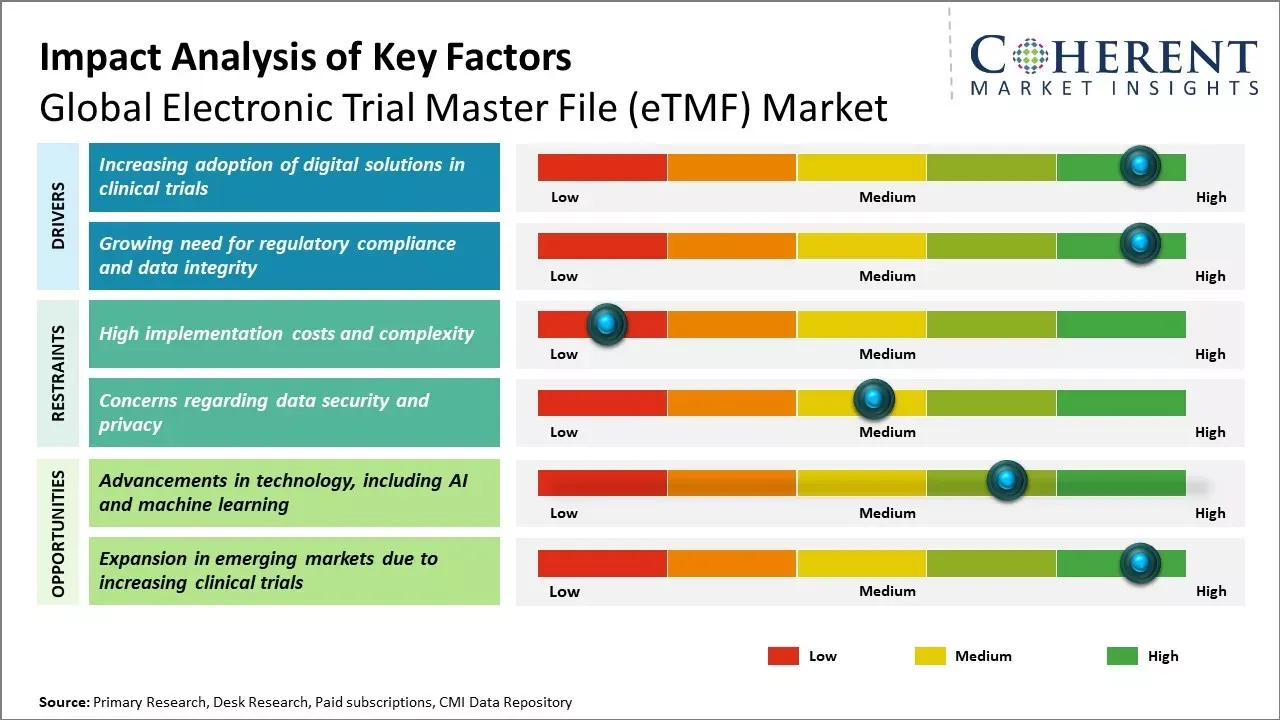
임상 시험에서 규제 준수가 점점 더 중요해짐에 따라 규제 제출 및 감사 준비를 용이하게 하는 전자 시스템에 대한 수요가 엄청났습니다. 제약 및 임상 연구 조직에서 디지털화 채택이 증가함에 따라 이러한 시스템을 통해 전 세계 임상 시험 현장에서 문서 관리 및 정보 검색이 더욱 효율적으로 이루어집니다.
그러나 높은 구현 비용과 복잡성으로 인해 전 세계 eTMF(전자 시험 마스터 파일) 시장 성장이 방해를 받을 수 있습니다.
시장 농축 및 경쟁력

이 보고서에 대해 자세히 알아보세요, 무료 샘플 다운로드
- Veeva Systems, Phlexglobal 및 IQVIA와 같은 전자 시험 마스터 파일 (eTMF) 시장에서 선도하는 회사는 포괄적 인 클라우드 기반 플랫폼 및 통합 임상 솔루션을 갖춘 업계를 지배합니다. 예를 들어, Veeva Systems는 글로벌 규제 프레임 워크 (예 : 미국 식품 및 의약품 관리 21 CFR Part 11, EU Annex 11)와 관련하여 eTMF 솔루션을 지속적으로 업데이트하여 고객 실시간 검사 및 자동화 감사 트레일을 제공합니다.
- eTMF 공간의 Mid-tier 기업은 비용 효율과 공정 효율을 우선화합니다. 이 회사는 종종 소유 시스템의 높은 투자없이 규제 준수를 찾는 소형 바이오 기술 및 제약 회사를 제공합니다. 지역 CRO와 전략적 파트너십을 맺고 해상 개발 팀을 활용하여 비용을 제어합니다. 예를 들어, MasterControl 및 ePharmaSolutions 대상 중형 스폰서와 같은 회사들은 customizable, GCP 규정 준수를 충족하는 확장 가능한 eTMF 도구를 제공하여 나머지 예산 친화적입니다.
현재 이벤트와 그 영향
현재 행사 | 묘사와 그것의 충격 |
규제 현대화 이니셔티브 |
|
기술적인 Disruptions |
|
75개 이상의 매개변수에 대해 검증된 매크로와 마이크로를 살펴보세요: 보고서에 즉시 액세스하기
임상 시험에서 Digital Solutions의 승인
제약 및 생명 과학 산업은 디지털 기술의 발전 때문에 엄청난 변화를 겪었습니다. 전통적으로 수행 된 임상 시험은 이제 디지털 솔루션으로 전환됩니다. 잠재적으로 환자의 안전과 지연 발달 시간을 질감할 수 있는 중요한 문서의 위험이 있었습니다.
예를 들어, Applied Clinincal Trials의 연구에 따르면, 6 월 2025, USD 1.05 백만은 AI / ML 사용 평가에 의해 AI / ML 사용에 투자되었으며, 팀은 AI / ML을 사용하여 18%의 평균 시간 감소를 경험했으며, 전반적으로 응답자는 약물 개발에서 AI / ML의 사용을 긍정적 인 전망보고했습니다.
규제 준수 및 Data Integrity에 대한 성장 필요
엄격한 규제 표준을 준수하고 최고 수준의 데이터 무결성을 유지하기위한 임상 시험 관리는 약물 개발 과정에서 중요합니다. 문서는 잘못 될 수, 데이터 transcription 오류가 발생할 수 있는 동안 전송 정보를 시스템. 종이 파일의 거대한 볼륨을 포함하는 규제 감사는 문서 검색에 도전하고 지연이 발생했습니다. 임상시험의 글로벌화를 통해 국가별 규정에 따라 당국에 대한 준수를 민주화하는 것은 논문과 도전이었습니다.
전자 시험 마스터 파일 (eTMF) Market Insights, Deployment Mode - Cloud-Based eTMF Solutions의 유연성과 확장성 향상
배포 모드의 관점에서 클라우드 기반 세그먼트는 가장 높은 시장 점유율에 기여할 것으로 예상됩니다. 62.6% 할인 2025년에, 그것의 융통성 및 확장성에 owing.
Cloud 기반 eTMF 솔루션은 생명 과학 조직, 특히 소규모 기업 및 CRO를 허용하여 온프레미스 구현과 관련된 대형 업 프론트 인프라 비용을 방지합니다. 클라우드 호스팅 서비스에 대한 연간 또는 월간 구독료를 지불합니다. 이 자본 지출 모델은 eTMF 기술을 더 많은 비용 감지 고객을 위해 접근 할 수 있습니다.
Electronic Trial Master File (eTMF) Market Insights, by Functionality - Workflows의 표준화는 문서 관리 기능에 대한 수요를 증가시킵니다.
기능 측면에서 문서 관리 부문은 가장 높은 시장 점유율에 기여할 것으로 예상됩니다. 40.8% 할인 2025년, 문서 제어의 표준화, 준수 프로세스의 필요성 때문에.
임상시험 및 제품 개발 프로젝트는 규제 표준에 따라 무결성과 추적성이 보장되어야 수많은 문서를 포함합니다. 종이 기반 시스템은 문서의 오류가 발생하고, 개정을 잃고, 소거 데이터 품질에 대한 일관성을 주장한다.
전자 시험 마스터 파일 (eTMF) 시장 통찰력, End User - 규정 준수 수요 제약 회사에서 eTMF Adoptions
최종 사용자의 관점에서 제약 회사 세그먼트는 가장 높은 시장 점유율에 기여할 것으로 예상됩니다. 49% 할인 2025년에, 기업 내의 엄격한 규칙에 owing.
글로벌 제약 제조업체는 공공 보건 당국의 강렬한 scrutiny를 직면하여 새로운 제품의 안전성과 효능을 입증합니다. 임상시험 및 규제준수의 적절한 수행을 보장하는 컴퓨터 시스템은 이러한 조직의 비즈니스 크리티컬이 됩니다.
전자 시험 마스터 파일 (eTMF) 시장의 혁신
- 자동화 및 인공지능의 통합 증가
제품 설명:: eTMF의 기계 학습 및 인공 지능 (AI)의 응용 프로그램은 크게 성장했습니다. 이 기술은 문서 적색, 메타데이터 태그 및 분류를 포함한 반복 프로세스를 자동화하는 데 더 많은 것을 사용했습니다. 더 빠른 문서 처리, 더 적은 인간적인 과실 및 더 전반적인 임상 시험 문서 관리 효율성은 이 자동화의 결과입니다.
이름 *: 11 월 2024에서 Veeva 시스템은 Vault CRM을 발표했습니다. Bot 및 Vault CRM 음성 제어, Vault CRM의 두 가지 새로운 GenAI 기능. Veeva Commercial Summit Europe에서 발표 된 CRM Bot 및 Voice Control은 Vault CRM에 다음해 새로운 혁신의 호스트에 참여합니다. 이러한 새로운 기능을 통해 기업들은 현장 생산성 향상을 통해 즉각적인 가치를 제공할 수 있습니다.
- 향상된 Data Integrity를 위한 블록체인 기반 감사 트레일
제품 설명:: 또 다른 신흥 혁신은 eTMF 시스템 내에서 immutable, time-stamped Audit trails를 만들 수있는 블록 체인 기술의 사용입니다. 미국 식품의약품안전처(FDA)와 같은 규제 기관은 추적성 및 탈염된 데이터의 중요성을 강조합니다. 블록 체인은 문서 또는 메타 데이터 필드에 대한 모든 수정을 영구적으로 기록하고 시간이 지남에 따라 거의 불가능합니다. 이것은 여러 이해 관계자 액세스 및 지역별 시험 문서를 수정하는 분산 임상 시험에서 특히 중요합니다.
이름 *: Startups 및 R&D 팀은 각 트랜잭션이 문서 업로드, 검토 또는 승인이 분산 ledger에 안전하게 기록되는지 여부를 파악하는 Blockchain-enabled eTMF 시스템을 조종합니다. Triall과 같은 기업은 멀티 사이트 및 원격 임상 시험에서 투명성과 규제 신뢰를 강화하기 위해 이것을 탐구하고 있습니다.
전자 시험 마스터 파일 (eTMF) 시장에 AI의 영향
전자 시험 마스터 파일 (eTMF) 임상 시험의 관리는 AI-powered 솔루션에 의해 혁명적입니다.
- 예측 분석: AI 프로그램은 가능한 탈선, 위험 및 병목을 예측하기 위해 과거 시험 데이터를 살펴. 본과 트렌드를 식별함으로써, 이러한 시스템은 유능한 의사결정을 가능하게 하고, 이해관계자가 더 심각한 문제가 될 수 있도록 합니다.
- 자연적인 언어 가공 (NLP): NLP를 사용하는 시스템은 문서의 압축 텍스트에서 귀중한 정보를 추출합니다. 이에는 정보 분류, 침술 분석 및 핵심 용어 식별이 포함됩니다. NLP는 문서 색인, 검색성 및 추세 분석을 향상시킵니다.
- 자동화된 문서 Categorization: AI 기반 알고리즘을 사용하여 컨텐츠에 따라 자동으로 분류 및 태그 문서, eTMF 내부 문서에 제대로 배열하는 데 필요한 수동 노동의 양이 감소됩니다. 이 문서는 제대로 배열되어있어 접근성과 조직을 향상시킵니다.
지역 통찰력

이 보고서에 대해 자세히 알아보세요, 무료 샘플 다운로드
북미 전자 시험 마스터 파일 (eTMF) 시장 분석 및 동향
북미는 전 세계 전자 시험 마스터 파일 (eTMF) 시장의 지배적 인 지역으로 확고하게 설립되었습니다. 35.9% 할인 2025년 임상시험에 대한 의료 인프라 및 엄격한 규정을 통해 미국과 캐나다는 제약 연구 및 개발 활동의 핵심 허브로 출범했습니다.
예를 들어, Novotech CRO에 의해 출판된 기사에 따르면, 2025년까지 인공 지능은 시험 데이터 작업의 50 %를 관리하고, 20 %의 시간을 절단하고 데이터 정밀도를 향상시킵니다. 이 AI 기반 효율은 복잡한 글로벌 평가에서 더 빠른 통찰력과 의사결정을 가능하게합니다.
아시아 태평양 전자 시험 마스터 파일 (eTMF) 시장 분석 및 동향
아시아 태평양 지역은 전자 시험 마스터 파일 (eTMF)에 가장 빠르게 성장하는 시장이 될 것입니다. 중국, 인도 및 대한민국과 같은 여러 개발 국가들은 점점 글로벌 임상 시험 대상이 되고, 더 낮은 비용과 큰 환자 풀을 빚고 있다.
예를 들어, 임상 리더에 의해 보고서에 따르면, 호주의 임상 시험은 미국과 유럽보다 30 % - 40% 덜 비쌉니다. 이 비용 차별은 중앙 집중식 및 지역 연구소에서 의사와 병원 비용으로 전체 연구 과정을 경간합니다. 호주는 다양한 환자 인구와 최고 수준의 의료 인프라 시스템을 제공합니다.
미국 전자 시험 마스터 파일 (eTMF) 시장 분석 및 동향
미국, Veeva Systems, Phlexglobal, IQVIA와 같은 선도적 인 eTMF 제공 업체는 주요 제약 회사 및 계약 연구 조직 (CRO)을 제공하는 중요한 시장 점유율을 보유합니다.
이 회사는 지속적으로 R & D에 투자하여 엄격한 미국 식품 및 의약품 관리 규정과 같은 21 CFR Part 11, 자동화 된 감사 트레일, 실시간 검사 읽음 및 향상된 보안 프로토콜과 같은 기능에 초점을 맞추고 있습니다. 이 플랫폼은 검증된 확장성, 규제 준수 및 광범위한 임상 시험 관리 시스템과 통합되어 널리 채택됩니다.
중국 전자 시험 마스터 파일 (eTMF) 시장 분석 및 동향
중국의 급속한 확장 약제 연구 및 개발 분야 및 국내에서 실시한 임상 시험의 증가 수는 eTMF 채택을 위한 중요한 운전사입니다. National Medical Products Administration (NMPA)는 국제 표준과 긴밀하게 연계하여 전자 문서 관리 시스템을 채택하기 위해 중국 스폰서 및 CRO를 푸시하여 준수 및 효율성을 향상시킬 수 있도록 최신 규정을 가지고 있습니다. 또한, 정부는 혁신과 디지털 건강 인프라를 지원하는 이니셔티브는 eTMF 기술에 투자를 증가시키기 위해 기여하고, 중국을 높은 성장 시장으로 위치.
Japan Electronic Trial Master File (eTMF) 마켓 분석 및 트렌드
일본 제약 산업은 고품질의 임상 데이터 관리 및 새로운 치료를위한 신속한 적시에 시장, 정교한 eTMF 솔루션에 대한 수요를 운전. 일본 규제 기관, 제약 및 의료 기기 기관 (PMDA), 위임 엄격한 문서 표준, 시운전 시험 마스터 파일 관리 및 검사 준비를 간소화하는 전자 시스템을 채택하는 현지 회사. 또한, 일본은 글로벌 다재다능한 임상시험에 참여하여 상호 운용성 및 준수 eTMF 플랫폼에 필요한 연료를 공급합니다.
캐나다 전자 시험 마스터 파일 (eTMF) 시장 분석 및 동향
캐나다의 성장 임상 연구 분야는 점점 데이터 무결성 및 감사 읽기를위한 건강 캐나다의 엄격한 요구 사항에 의해 구동되는 eTMF 시스템을 채택하고 있습니다. 환자 안전 및 준수에 강한 초점으로, 캐나다 스폰서 및 CROs는 보안, 탬퍼 증거 문서를 보장하고 규제 검사를 촉진하는 eTMF 솔루션을 우선 순위.
가격 분석
중소기업
- 가격 일반적으로 사용 및 기능에 따라 USD 1,000에서 USD 5,000의 범위. 기본 패키지는 USD 500 / 월만큼 낮을 수 있지만 일반적으로 용량 또는 기능을 가지고 있습니다.
큰 기업 및 CROs
- 비용은 기업 수준의 지원, 사용자 정의 구성 및 다중 사용자 라이센스를 갖춘 포괄적 인 통합 플랫폼을위한 월 10,000 ~ USD 50,000 +에 도달 할 수 있습니다.
- 이름 *
- Veeva Systems는 전형 사용자 및 per-study 기반에 대한 전형적 책임이며, 엔터프라이즈 계약은 높은 사용자 정의 및 통합을 반영하여 프리미엄 가격 솔루션을 만듭니다.
- MasterControl 및 Phlexglobal와 같은 Mid-tier 제공 더 유연한 가격, 중소형 생명 공학 및 더 작은 CROs 클라이언트 필요에 따라 스케일링 기능 및 스토리지에 의해.
- 이름 *
시장 보고서 Scope
전자 시험 마스터 파일 (eTMF) 시장 보고서 적용
| 공지사항 | 이름 * | ||
|---|---|---|---|
| 기본 년: | 2024년 | 2025년에 시장 크기: | USD 3.00 원 |
| 역사 자료: | 2020년에서 2024년 | 예측 기간: | 2025에서 2032 |
| 예상 기간 2025년에서 2032년 CAGR: | 12.6% 할인 | 2032년 가치 투상: | USD 3.00 바트 |
| 덮는 Geographies: |
| ||
| 적용된 세그먼트: |
| ||
| 회사 포함: | Veeva Systems Inc., Medidata Solutions, Inc., Oracle Corporation, Parexel International Corporation, IBM Watson Health, DrugDev (현재 Veeva의 일부), MasterControl, Inc., ArisGlobal LLC, Dassault Systèmes, Trial Interactive, Signant Health, Forte Research Systems, Inc., Axiom Real-Time Metrics, eClinical Solutions, LLC 및 Bioclinica, Inc. | ||
| 성장 운전사: |
| ||
| 변형 및 도전 : |
| ||
75개 이상의 매개변수에 대해 검증된 매크로와 마이크로를 살펴보세요: 보고서에 즉시 액세스하기
글로벌 전자 시험 마스터 파일 (eTMF) 산업 뉴스
- 4월 2025일 스낵 바 시스템은 Veeva SiteVault CTMS, SiteVault eISF 및 SiteVault eConsent와 통합되는 연구 사이트의 임상 시험 관리 시스템인 Veeva SiteVault CTMS를 발표했습니다. Veeva의 임상 Platform을 사용하여 스폰서와 통합은 수동 프로세스를 줄이고 효율성을 높일 수 있도록 스폰서들에게 원활한 양방향 데이터 흐름을 제공합니다.
- 2월 2025일 Oracle 생명 과학 Everest Group Life Sciences Clinical Trial Management System (CTMS) 제품 PEAK Matrix Assessment 2024의 ‘Leader’로 선정되었습니다. 이 설계는 Oracle의 지속적인 노력으로 의료 시스템 및 생명 과학 조직을 지원하도록 설계된 혁신적이고 비용 효율적인 솔루션을 통해 임상 시험 관리를 변환하는 것입니다.
- 5월 2025일, CDISC + TMF 유럽 최근 제네바에서 열린 인터체인지, 업계 리더, 전문가 및 혁신가들이 특정 평가 마스터 파일 (TMF) 관리 트랙과 함께 임상 시험의 진화 풍경에 대해 논의했습니다. 올해는 임상 데이터 교환 표준 컨소시엄 (CDISC)가 형성 된 이후 25 년이 표시되어 여러 테마와 뜨거운 주제를 강조하는 이벤트가 업계 전반에 걸쳐 명확하게 공유됩니다.
- 4 월 2025에서 Medidata Solutions는 Medidata Rave eTMF 2025.1.0의 출시를 발표했습니다.
항문핥기
- 글로벌 전자 시험 마스터 파일 (eTMF) 시장 성장은 CRO에 대한 임상 시험 활동의 상승에 의해 추진되고 운영 효율성을 개량하는 그들의 성장 초점. 엄격한 규제 요구 사항은 적절한 문서 보관 및 임상 문서에 대한 원격 액세스가 시장 성장을 구동 할 수 있습니다.
- 북미는 예측 기간 동안 시장을 지배 할 것으로 예상됩니다. 높은 임상 연구 지출 및 엄격한 규제 요구 사항은 지역 CRO 및 제약 회사의 대부분을 구동하여 프로세스를 디지털화합니다. 유럽은 지속적인 약물 개발 활동으로 인해 글로벌 전자 시험 마스터 파일 (eTMF) 시장에서 탁월한 지역입니다.
- 아시아 태평양 지역은 빠르게 성장하는 지역이 될 것으로 예상되며 중국과 인도와 같은 국가에서 임상 시험 아웃소싱 활동의 급속한 확장으로 인해 eTMF 공급 업체의 가장 유망한 기회를 제공 할 것으로 예상됩니다.
- 임상 시험은 전 세계 일어나고 있으며, eTMF 시스템은 다른 국가의 규칙과 유지해야하며, 뒤에는 떨어질 것입니다. 동시에 AI는 스마트 도구없이 모든 시스템을 변경하고 위험에 대한 실시간 데이터가 지속되지 않습니다. 미래는 AI 힘과 글로벌 규칙을 결합하는 사람들에 속합니다. 다른 사람은 뒤에 떠난다.
- 지역별 데이터 개인 정보 보호 및 규제 변화는 전 세계 eTMF 회사에 도전할 수 있습니다. 클라우드의 민감한 환자 데이터를 저장하는 데 관련된 보안 문제는 시장의 성장을 해커 할 수 있습니다. 전통적인 종이 기반 시스템에 비해 임상 문서의 전자 아카이브의 장점에 대한 인식은 eTMF 솔루션에 대한 수익성을 제공 할 수 있습니다.
공유
저자 정보
Monica Shevgan은 상임 경영 컨설턴트입니다. 그녀는 정보 및 통신 기술 분야의 전문 지식을 바탕으로 시장 조사 및 비즈니스 컨설팅 분야에서 13년 이상의 경험을 보유하고 있습니다. 전략적 의사 결정에 도움이 되는 고품질 통찰력을 제공한 실적을 바탕으로, 그녀는 조직이 비즈니스 목표를 달성하도록 돕는 데 전념하고 있습니다. 그녀는 첨단 기술, 엔지니어링, 운송을 포함한 다양한 분야에서 수많은 프로젝트를 성공적으로 저술하고 멘토링했습니다.
독점적인 트렌드 보고서로 전략을 혁신하세요:
자주 묻는 질문