위험 기반 모니터링 시장 크기와 예측 – 2025 – 2032년
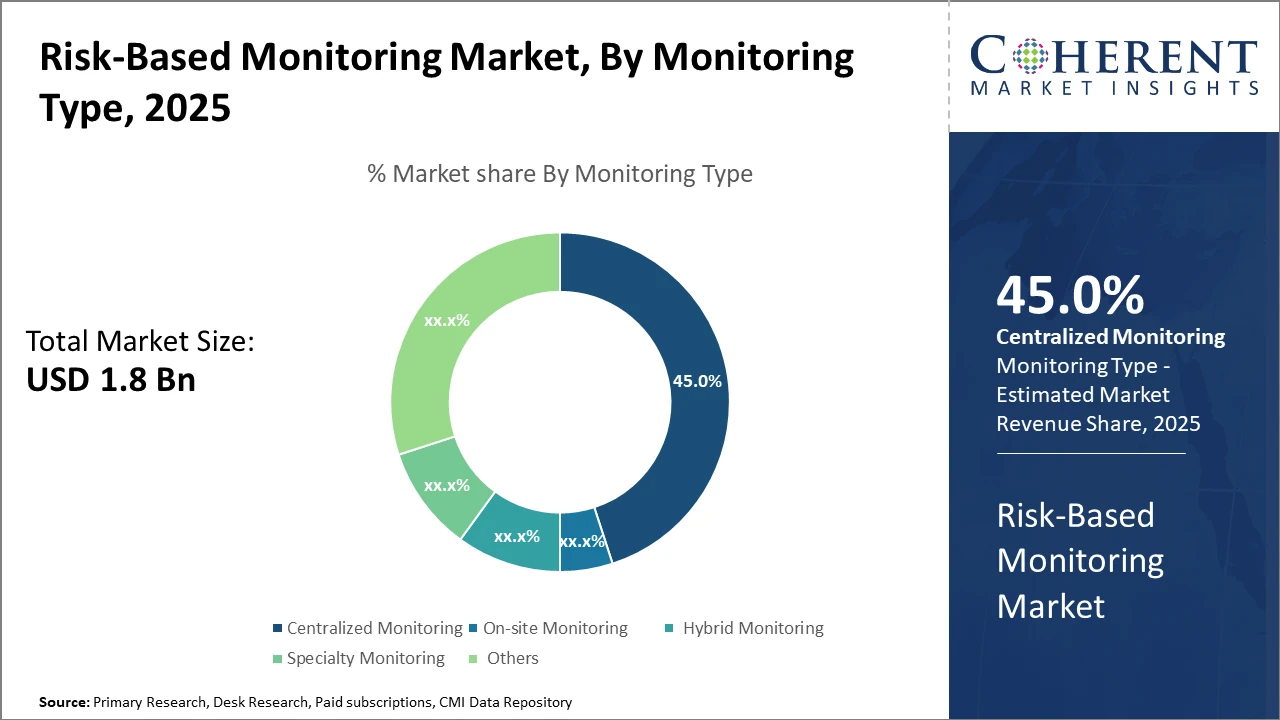
글로벌 위험 기반 모니터링 시장 크기는 추정된다 2025년 USD 1.8 억에 달하며 USD 3.2에 도달 할 것으로 예상됩니다. 2032년까지 수십억 달러의 합성 연간 성장률 (CAGR)을 8.2% 전시 2025에서 2032까지.
제품정보
위험 기반 모니터링 제품은 소프트웨어 플랫폼 및 분석 임상 시험, 품질 시스템 및 규제를 감독하는 데 사용되는 도구 준수 활동. 이 솔루션은 높은 리스크 프로세스를 우선 순위, 사이트, 또는 알고리즘을 사용하는 데이터 포인트, 실시간 분석 및 중앙화된 대시보드. 위험 기반 모니터링 제품 도움말 조직은 자원 할당을 최적화, 데이터 무결성을 향상, 및 초기 증상을 감지합니다. 일반적으로 자동화 된 경고를 포함, 통계 모델링, 감사 트레일 및 임상 데이터 통합 관리 시스템.
키 테이크아웃
중앙화된 감시는 45%를 가진 감시 유형 세그먼트를 지도합니다 그것의 비용 효율성 및 포괄적인 oversight 때문에 시장 점유율 하이브리드 모니터링은 가장 빠르게 성장하는 역할을 합니다. 유연한 모니터링 솔루션에 대한 수요 증가로 구동되는 접근. 특수 모니터링을 포함한 다른 형태, 틈새 해결을 계속 임상 시험 필요조건.
제약 회사는 최종 사용자 채택, 반사 광범위한 임상 파이프라인; 학술 및 연구 기관, 그러나, 확장하여 가장 빠르게 성장하는 최종 사용자입니다 번역 연구 노력.
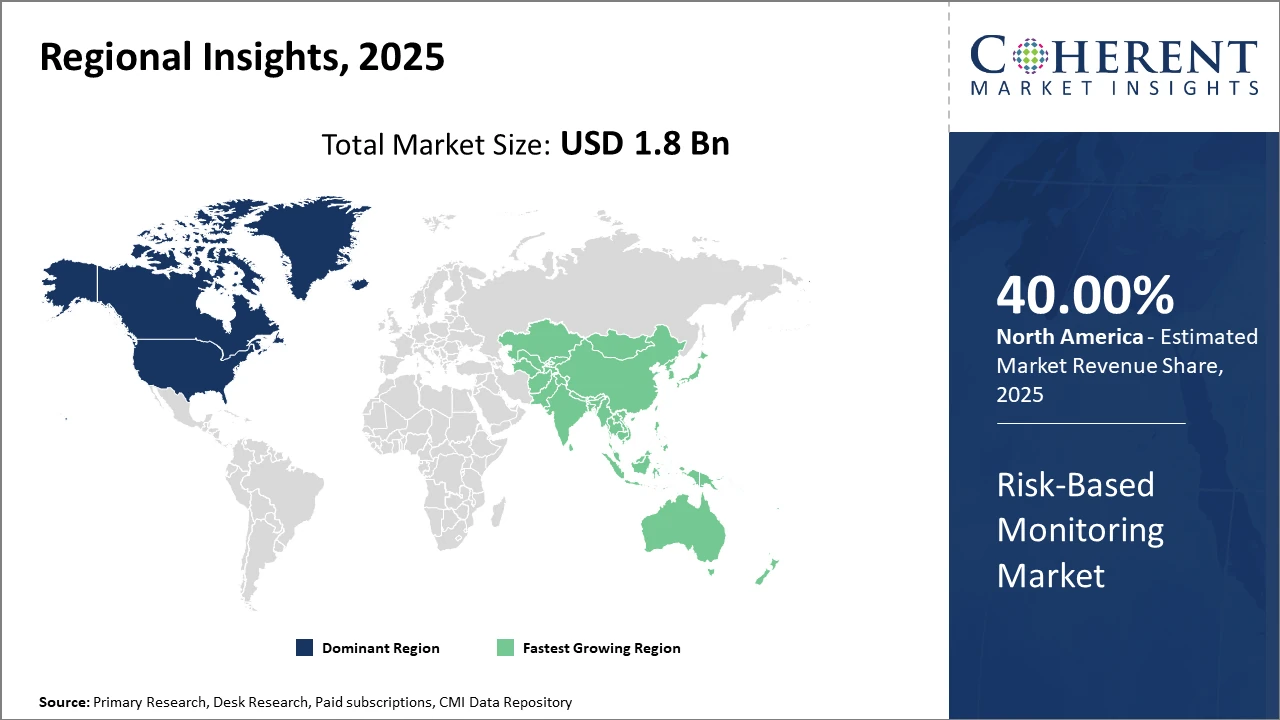
북미는 규제에 가장 큰 시장 점유율을 보유 프레임 워크 및 고급 의료 인프라, 아시아 동안 태평양은 가장 빠르게 성장하는 지역이며, 임상 시험 상승 아웃소싱 및 정부 이니셔티브.
유럽은 엄격한 규제 준수를 레버리지, notable RBM 도구를 향상시키기 위해 시장 선수 중 협업 노력 GDPR 및 기타 개인 정보 보호법에 따라.
위험 기반 모니터링 시장 세그먼트 분석
이 보고서에 대해 자세히 알아보려면: 무료 샘플 다운로드
위험 기반 모니터링 시장 통찰력, 모니터링 제품정보
중앙화 된 모니터링은 시장 점유율을 45%, 덕분에 포괄적 인 원격 통찰력과 비용 절감을 제공 할 수있는 능력 전통적인 현장 접근법과 비교. 단지의 상승 다중 중심 연구는 더 집중된 수요를 가지고 있습니다 솔루션. Hybrid Monitoring은 가장 빠르게 성장하는 subsegment입니다. 원격으로 현장 방문을 결합 자료실 관련 기사 위험 완화에 유연성을 보장하기 위해 자원 할당을 최적화. 현장 모니터링은 계속 주소 규제 요건 및 고위험 프로토콜, 특수 모니터링 oncology와 같은 특별 한 재판, 그리고 다른 사람 커버 신흥 혁신적인 모니터링 방법론.
위험 기반 모니터링 시장 통찰력, By 끝 사용자
제약 회사 명령으로 인해 가장 큰 시장 점유율 글로벌 평가 포트폴리오 및 중요한 R & D 예산. RBM을 구축하여 운영 규정 준수 효율성. 학술 및 연구 연구소는 가장 빠른 성장 subsegment, 번역 연구 증가에 의해 구동 위험 기반 준수 프레임 워크를 요구하는 연방 수익 프로젝트. CROs는 여러 매체로 행동하여 꾸준한 성장을 유지합니다. 스폰서. 생명 공학 회사는 온건한 uptake를 보여줍니다, 에 집중 초기 임상 연구, 다른 사람들은 틈새 선수를 대표하면서 비-traditional 임상 신청을 위한 RBM 채택.
위험 기반 모니터링 시장 통찰력, 배포 모델 번호:
Cloud 기반 배포는 급속하게 견인력을 얻는다. 확장성, 낮은 상승 비용 및 실시간 협업 다양한 시장의 경쟁력 강화 선수. 이 subsegment는 가장 빠른 성장의 위치를 보유 배포 모드, 향상된 데이터 보안 프로토콜 및 용이성에 의해 추진 다른 클라우드 고유의 eClinical 시스템과의 통합. 온-프레미스 솔루션은 엄격한 데이터와 조직의 선호도 유지 관리 정책 또는 유산 시스템 투자, 웹 기반 플랫폼은 사용자 친화적 인 인터페이스를 제공합니다. 조직 및 분산 된 재판.
위험 기반 모니터링 시장 동향
위험 기반 모니터링 풍경은 점점 더 구동됩니다. 기계 학습 알고리즘 및 클라우드와 같은 기술 혁신 컴퓨팅, 동적 위험 식별 및 완화를 가능하게합니다.
예를 들어, AI-enabled RBM 플랫폼은 2024 제안에서 시작되었습니다. 모니터링이 감소한 예측 분석 30%의 강화 효율성.
또한, 분산 임상 시험의 상승 pandemic 유도 디지털 의료 가속에 의해 촉진 propels 시장 진화.
가상 사이트 평가를 위한 AR 배포 안내서가 개선되었습니다. 물리적 존재없이 oversight를 후원, 최근 2025에 의해 발굴 기술 공급자와 약제 사이 협력 스폰서.
이 동향은 전통적인 현장의 시장 변화에 서명합니다. 패러다임 모니터링, 기술 지원 프레임 워크.
위험 기반 모니터링 시장 통찰력, By 한국어
이 보고서에 대해 자세히 알아보려면: 무료 샘플 다운로드
북미 위험 기반 모니터링 시장 분석 및 연락처
북미에서 위험 기반 모니터링 시장의 지배 vigorous 임상 연구 활동에, 전적으로 FDA를 포함한 강력한 규제 생태계에 의해 지원되는 미국 위험 기반 접근을 촉진하는 가이드. top-tier의 존재 제약 회사 및 CRO 본사 더 연료 수요. 시장 수익의 약 40 %가 2025로 생성됩니다. 초기 기술 채택 및 광범위한 임상 시험에 의해 구동 볼륨.
아시아 태평양 위험 기반 모니터링 시장 분석 및 연락처
한편, 아시아 태평양은 CAGR와 가장 빠른 성장을 전시 2025에서 2032까지 10 %를 초과합니다. 정부 주도의 이니셔티브 임상시험, 향상된 의료 인프라, CRO 확장 존재는 RBM 채택을 격려합니다. 국가 같은 중국과 인도는 증가 아웃소싱 및 제품정보 건강정보 통합, 진화 시장에 기여 생태계.
Key 용 위험 기반 모니터링 시장 전망 국가 *
미국 위험 기반 모니터링 시장 분석 및 연락처
미국의 위험 기반 모니터링 시장은 상당한 확장을 반영합니다. 초기 규제 인식 및 디지털 건강 투자에 의해 원조. 리드 산업 참가자는 고급 RBM 센터를 설립했습니다. AI 중심의 솔루션으로, 시험 주기 시간을 단축하여 25% 에 2024. 연방 기관과 협력 이니셔티브 개인 entities는 표준화 RBM 프레임 워크에 중점을두고 있습니다. 국가의 시장 점유율을 제안합니다. 또한, 광대 매사추세츠와 캘리포니아 바이오텍 허브의 임상시험량 bolster 수요.
중국 위험 기반 모니터링 시장 분석 및 연락처
중국 정부의 위험 기반 모니터링 시장 혜택 임상 연구 oversight의 혁신을 촉진하는 인센티브. 더 보기 국가는 RBM 배포에서 35 % 년의 성장 이상을 목격했습니다. 2023년부터 지역 CRO와 국제 간의 파트너십을 주도 제약 회사. ο 수집항목 : 이름 , 생년월일 , 성별 , 로그인ID , 비밀번호 글로벌 가이드라인의 시험 기준은 RBM 채택을 가속화했습니다. telemedicine 인프라 및 AI에 투자하여 지원 신청.
항문 Opinion
위험 기반 모니터링 채택은 주로 수요 측에 의해 구동 임상 시험 참가자 수와 같은 지표 escalating complexity of 임상 프로토콜. 2024년, 50% 이상 대용량 단계 III 재판은 RBM 전략을 통합, 에서 상승 2022년에 40%, 임상시험 등록 자료에 따라, underscoring 성장 시장 점유율 잠재력.
RBM 도구의 상당한 확장을 강조 생산 능력, 글로벌 소프트웨어 배포 35% 상승 2025년에 년 이상. 가격 모델은 점점 더 이동 구독 기반 SaaS 제공, 감당성 및 uptake 강화 중형 임상연구기관 중.
약제의 맞은편 사용 케이스 신청, 생명 공학 및 의료 기기 분야는 RBM 성장 인공지능(AI) 및 원격 모니터링 통합 기술. 예를 들어, 2024년, AI 증강 RBM 사용 플랫폼 증가 평가판 사이트 모니터링 효율 25% 이상 산업 회의에서 보고.
Micro-level 지표는 지역 차이를 반영합니다. North 미국과 유럽은 엄격한 RBM 시장 매출을 선도합니다. 규제 요건. 아시아 태평양은 nascent를 보여줍니다. 아직 가장 빠르게 성장하는 수요가 정부 인센티브 및 임상 시험 아웃소싱 활동 증가.
시장 범위
| 공지사항 | 이름 * | ||
|---|---|---|---|
| 기본 년: | 2025년 | 2025년에 시장 크기: | 100억 |
| 역사 자료: | 2020년에서 2024년 | 예측 기간: | 2025에서 2032 |
| 예상 기간 2025년에서 2032년 CAGR: | 8.2% 할인 | 2032년 가치 투상: | 100억 |
| 덮는 Geographies: |
| ||
| 적용된 세그먼트: |
| ||
| 회사 포함: | Syneos 건강, PRA 건강 과학, 제약 제품 개발 (PPD), PharmaLex GmbH, eClinical Solutions, BenevolentAI, Capgemini, Indegene, 사마 기술, Medable Inc. | ||
| 성장 운전사: |
| ||
75개 이상의 매개변수에서 검증된 매크로와 마이크로를 발견하세요, 보고서에 즉시 액세스하세요
위험 기반 모니터링 시장 성장 요인
임상 시험의 성장 복잡성 더 RBM 시장 성장을 주도하는 정교한 모니터링 기술. 2024년에, 복잡한 적응 시험 설계는 거의 30%를 차지했습니다. initiated trials, 데이터 관리 필요성을 강화. 지원하다 규제 강조 위험 경고 회사연혁 FDA의 지침 업데이트와 같은 프레임 워크 EMA의 권장 사항 포스트-2023, RBM 통합 스폰서가 준수를 유지하십시오. 또 다른 키 드라이버의 발전 실시간 데이터 분석을 가능하게 하는 클라우드 기반 모니터링 플랫폼, 시험 모니터링 비용을 최대 20% 감소, 최근 관찰 단계 II 연구. 분산 임상 시험의 성장 투자 (DCTs) COVID-19 디지털 변혁 추세가 추가되었습니다. RBM 채택을 확장, 특히 신흥 지역에서 집중 telemedicine 인프라.
위험 기반 모니터링 시장 개발
4월 2024일 Oracle Health 출시 클라우드 기반 위험 기반 모니터링 (RBM) 플랫폼 AI 통합 정확도, 효율성 및 향상을 위해 설계된 기능 임상 시험 모니터링의 확장성. 해결책은 순간을 가능하게 합니다 위험 탐지, 집중된 oversight 및 자동화 분석, 도움 스폰서 및 CROs는 시험 품질을 강화하면서 운영 비용을 절감합니다. 및 규제 준수.
2022년에, 사이트맵AI/ML 기반 모니터링 솔루션 도입 TCS ADDTM 임상 분석 플랫폼은 어떻게 변화하는지를 목표로 합니다. 임상 시험은 감시됩니다. 해결책은 proactive 할 수 있습니다 고급 데이터를 통한 연구 및 사이트 수준의 위험 식별 분석, 지원 smarter 의사 결정, 개선된 환자 안전, 최적화된 시험 성능.
키 플레이어
시장의 선도 기업
Syneos 건강
PRA 건강 과학
제약 제품 개발 (PPD)
제약Lex 회사 소개
eClinical 솔루션
인기 카테고리
카테고리
연구분야
Saama 기술
회사 소개
몇몇 시장 선수는 같은 경쟁 전략을 채택했습니다 인공지능과의 전략적 파트너십을 통해 bolster 분석 기능 RBM 모듈을 더 넓은 eClinical 제품군에 통합합니다. 제품 정보 예, Veeva 시스템은 클라우드 기반 RBM 기능을 확장 늦은 2024, 6 내 클라이언트 인수의 15 % 증가 결과 달. 마찬가지로 Medidata의 AI 스타트업 Syneos 인수 예측 위험 득점, 빠른 규제 준수를 촉진. 이 이니셔티브는 크게 시장 성장 전략에 영향을 미쳤습니다. 더 높은 시장 점유율을 캡처 할 수 있습니다.
위험 기반 모니터링 시장 미래 전망
미래 성장은 임상 시험 복잡성을 증가하여 구동됩니다. 분산 및 하이브리드 시험 모델로 이동. 통합 인공지능, 실시간 분석 및 자동화 더 향상된 모니터링 효율. 규제 지원 및 비용 최적화 노력은 더 넓은 채용을 장려합니다. 제약 및 생명 공학 회사. 디지털 변환 생명 과학에서 계속, 위험 기반 모니터링이 될 것입니다 기업 기준.
위험 기반 모니터링 시장 과거 분석
제약으로 개발된 위험 기반 모니터링 시장 회사는 전통적인, 자원 집중에 대안을 모색 임상 시험 모니터링 방법. 초기, 규제 불확실성 제한된 채택, 그러나 데이터 분석 및 중앙화의 발전 모니터링 기술 향상된 합격. 시간 이상, 규칙 점점 증가된 위험 기반 접근, 인식 시험 효율성과 자료 질을 개량하는 잠재력. 옵션 정보 임상 시험으로 가속된 것은 더 복잡하고 세계적으로, 시장의 성장 trajectory를 강화.
이름 *
1차 연구 인터뷰:
임상시험 관리자
규정 준수
사이트맵 회사연혁
데이터 과학자
품질 보증 머리
데이터베이스:
GlobalData 임상 시험
Statista 생명 과학
FDA 인증 규제 데이터
EMA 임상 연구 보고서
잡지 :
적용 임상 시험
제약 기술
BioPharma 제품 사이트맵
임상시험
아웃소싱-Pharma
저널:
임상시험 논문
약물 정보 Journal
치료 혁신 및 규제 연구분야
임상연구
현대 임상 시험
협회 :
약정보협회
임상 연구 전문가 협회
FDA,
유럽 의학 기관
이름 *
공유
저자 정보
Manisha Vibhute는 시장 조사 및 컨설팅 분야에서 5년 이상의 경험을 가진 컨설턴트입니다. 시장 역학에 대한 강력한 이해를 바탕으로 마니샤는 고객이 효과적인 시장 접근 전략을 개발하도록 지원합니다. 그녀는 의료 기기 회사가 가격 책정, 환불 및 규제 경로를 탐색하여 성공적인 제품 출시를 보장하도록 돕습니다.
독점적인 트렌드 보고서로 전략을 혁신하세요:
자주 묻는 질문

