글로벌 Microbiome 치료 시장 크기와 예측 – 2026 에 2033
글로벌 microbiome 치료 시장은 성장할 것으로 예상됩니다. 100원 57.4 미크론 2026에서 50-100 원 2033년까지 화합물의 연간 성장률을 등록 (CAGR)의 3.6% 할인· microbiome therapeutics 시장은 중요한 확장을 위해, 항균성 (AMR)의 글로벌 부담 상승에 의해 연료를 공급됩니다.
Lancet의 연구는 항균 저항 (AMR)이 2021 년 전세계 추정 4.71 백만 사망에 연결되어 있다고보고, 그 중 1.14 백만은 항균 저항 (AMR)에 직접 발생했습니다. 예상은 항균 저항 (AMR)의 죽음이 2050에 의해 연간 거의 1.91 백만 증가한다는 것을, 총 사망 약 8.22 백만.
(출처: Lancet 소개·
또한 세계 은행은 항균 저항 (AMR)이 2050 달러에 의해 추가 의료 비용으로 USD 1 조에 결과 할 수 있으며 연간 글로벌 GDP 손실은 2030 달러에서 USD 3.4 조에 이르기까지 심각한 경제적 영향을 강조합니다.
(출처):: 세계은행·
Global Microbiome Therapeutics 시장의 주요 취항지
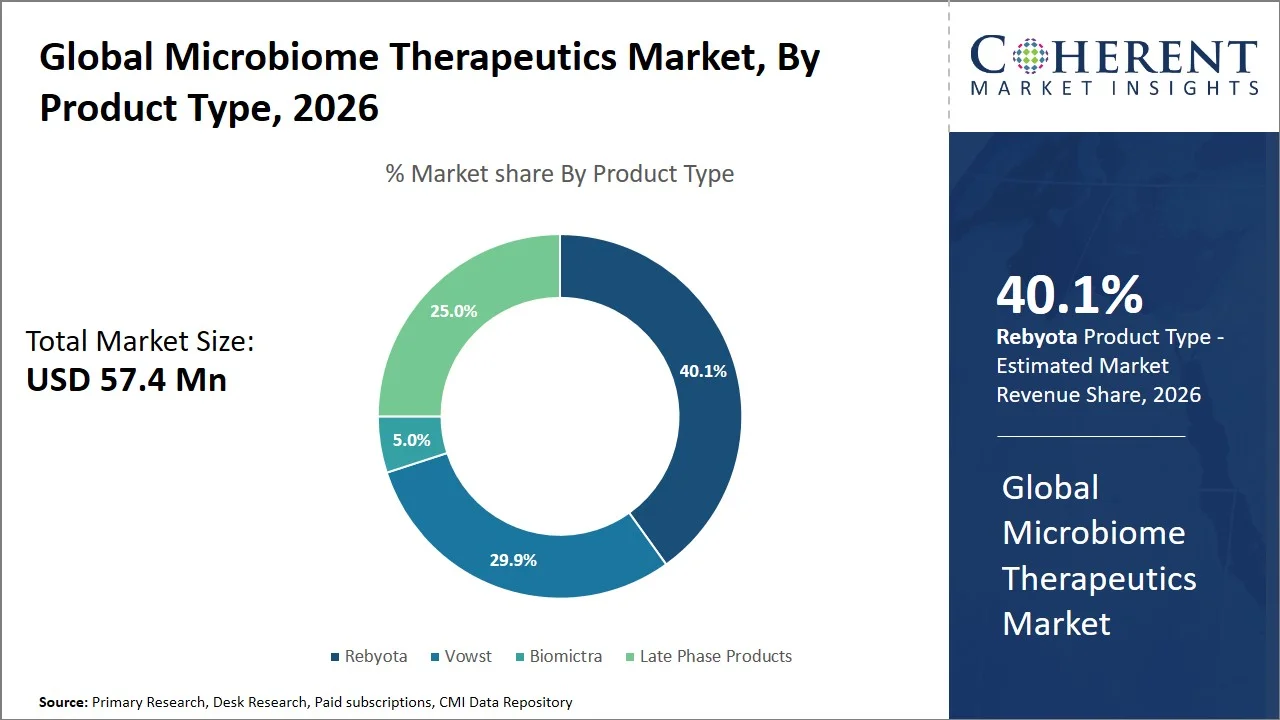
- Rebyota는 파악하기 위하여 계획됩니다 40.1의 100%년 2026년 글로벌 미생물 시장 점유율을 차지하고 있는 글로벌 마이크로비옴 치료제 시장은 미국 최초로 미국 FDA 승인된 마이크로비옴 약과 재순환 감염의 치료에 널리 보급된 광범위한 용도를 가지고 있습니다. 예를 들어, 11 월 2022에서 미국 식품 의약품 관리는 Rebyota, Ferring Pharmaceuticals의 제품에 녹색 빛을주었습니다. 이 승인은 미국에 허가 된 최초의 미생물 기반 치료였습니다. 약물은 항생제로 치료 된 후 성인에서 Clostridioides difficile 감염의 반환을 방지하도록 설계되었습니다. (출처: 식품 및 의약품 관리·
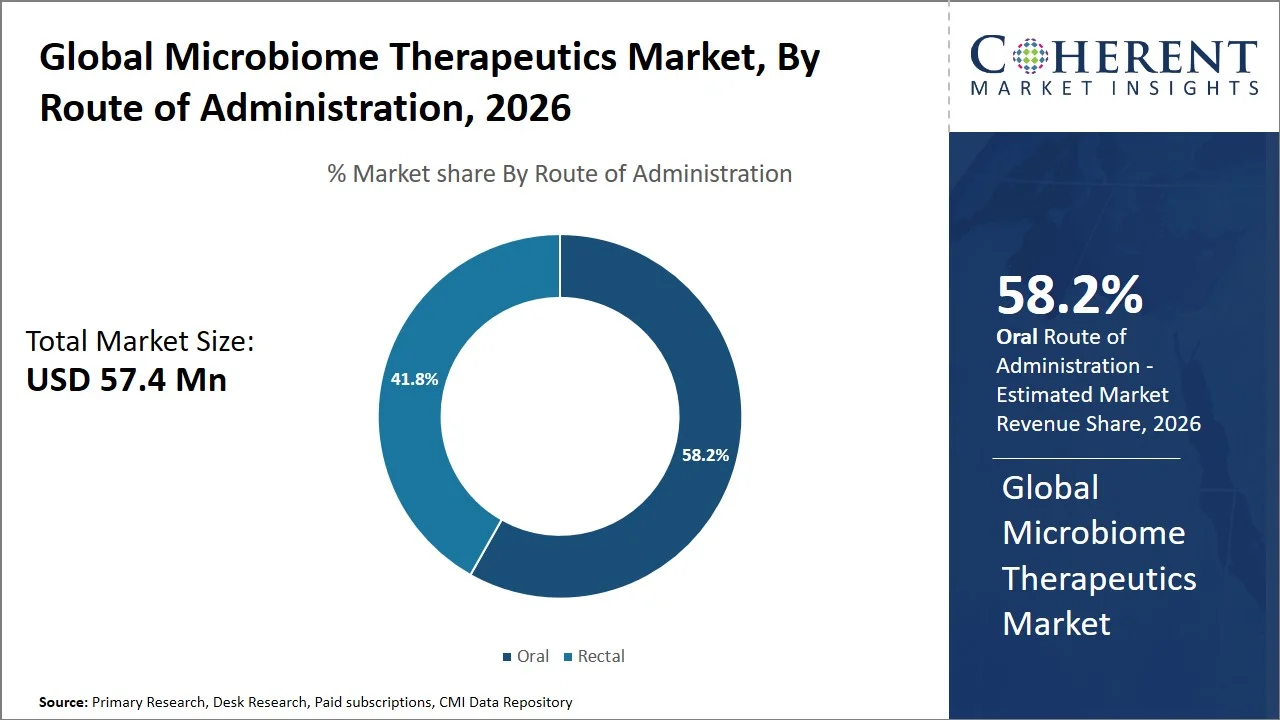
- 구두는 계획됩니다 58.2 원 100%년 글로벌 microbiome 치료 시장 점유율 2026, 관리 부문의 지배적인 경로 만들기. 북미 및 유럽은 세그먼트 내에서 상당한 성장을 목격하고, 향상된 환자 준수, 비침습적 응용 프로그램에 의해 연료를 공급하고, Vowst와 같은 구강 미생물 약물에 대한 승인을 증가시킵니다. 예를 들어, Vowst를 증발하는 임상 시험은 두드러지게 더 나은 환자 결과 및 편의성을 보여주었습니다. 특히 Clostridioides difficile 감염의 반복은 8 주 표에 위약 39.8%와 비교된 Vowst에 대략 12.4%가 있었습니다. 이것은 강력한 효과와 더 나은 환자의 고착을 나타내고, 관리의 구두, 비침범성 방법 때문에 가능성이 있습니다. (출처: 식품 및 의약품 관리·
- 병원 세그먼트는 파악하기 위하여 계획됩니다 47.0의 100%년 2026년 글로벌 마이크로비옴 치료 시장 점유율을 차지하고, 의료 시설의 고급 인프라로 인해 북아메리카의 지배적 인 치료 설정 세그먼트를 만들기 위해, 최근에 바이오매스를 출시하고, 임상 설정에서 미생물 기반 치료의 통제 된 납품에 대한 요구. 예를 들어, Mayo Clinic과 같은 전문 의료 및 연구 시설의 확장 및 Cleveland Clinic과 같은 기관의 전용 미생물 연구 및 치료 프로그램의 설립은 지역의 강력한 임상 인프라를 강조합니다.
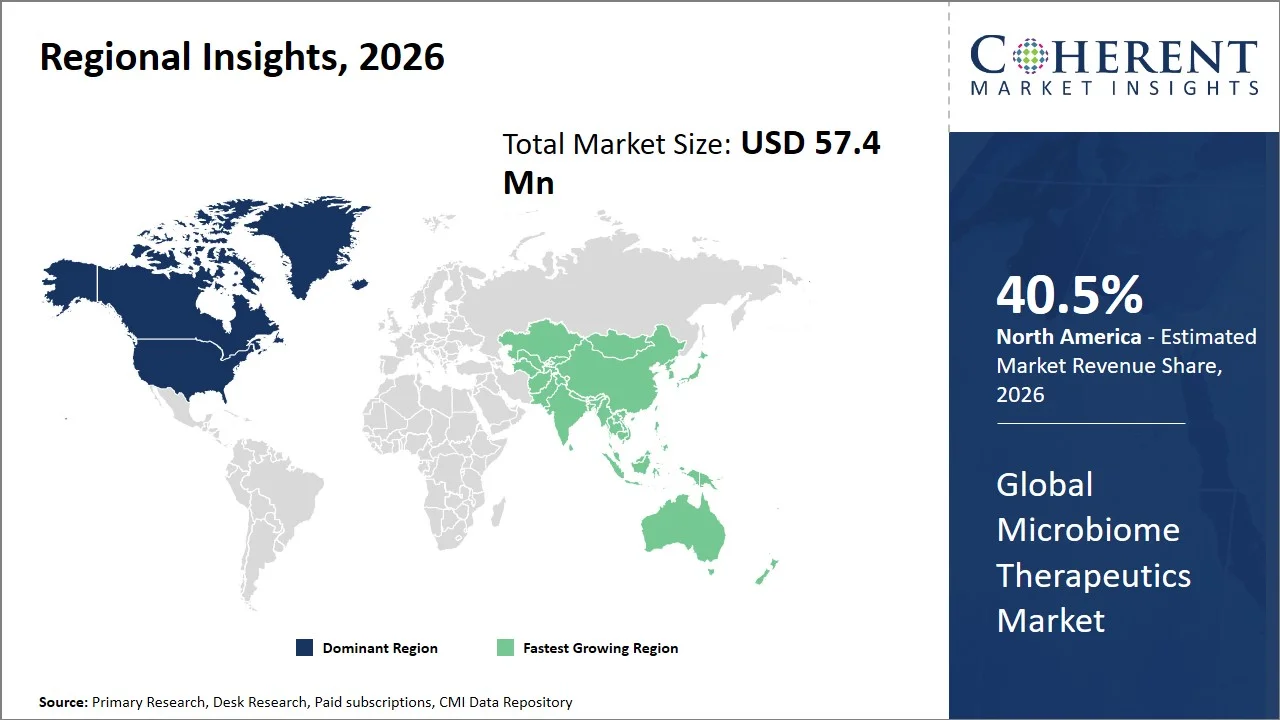
- 북미는 예상된 공유를 가진 지배력을 유지 40. · 5% 할인 2026년, 주로 미생물 기반 치료, 강력한 연구 노력 및 정교한 생물학적 치료의 초기 규제 승인으로 인해. 또한, 정부(e.g., Human Microbiome Project)가 지원하는 실질적인 미생물 기반 연구 노력과 함께 강력한 건강 관리 시스템의 가용성은 지역 내에서 상업적 성공을 촉진하는 데 도움이됩니다.
- Asia Pacific은 가장 빠르게 성장할 것으로 예상됩니다. 22. 기타 5% 할인 2026년, 바이오 기술 및 정밀 의학의 정부에 의해 증가된 강조의 결과로, 임상 시험 수행을 위한 증가된 수용량 및 sizable 참을성 있는 수영장은, 만성 질병을 가진 환자의 증가 수와 더불어, 규제 인프라에 있는 전진하고 genomics와 미생물 연구에 자금 조달은 시장 성장을 추진하고 있습니다. 예를 들어, 인도의 게놈 인도 프로젝트, Biotechnology 부서에 의해 뒷받침되는 주요 정밀 의학은 20 개 이상의 기관을 제공합니다. 프로젝트는 국가 게놈 데이터베이스를 만드는 목표로 10,000 이상의 게놈 샘플을 시퀀스했습니다. 이 데이터베이스는 고급 치료 및 미생물 연구에 대한 자원 역할을합니다. (출처: Genome 인도·
- Oncology에서 Adjunct 치료로 확장:: 암 치료 면역 요법은 미생물을 개선 할 수있는 지역으로 점점 관심을 얻고 있습니다. 결과적으로, 틈새는 암 치료에서 이용된 검문소 억제물의 효능을 강화하는 조합 치료에서 신흥됩니다.
- 구강 캡슐 기반 Microbiome 개발 치료사: 침략 사이트맵 표준 구두 캡슐 납품에 이식 절차는 수락과 사기를 강화하고 있습니다. 이 개발은 수익성과 편리한 미생물 기반 약물에 대한 틈새 영역을 만듭니다.
왜 Rebyota는 글로벌 Microbiome 치료법을 지배합니다. 시장?
Rebyota는 시장 점유율을 파악하기 위한 계획입니다. 40.1% 할인 2026 년, 표준화 된 라이브 바이오 치료 제품 (LBP)로 설립 된 규제 경로 및 임상 검증에 의해 substantiated, 이후 미생물 기반 치료에 대한 모델을 설립. 미국 식품의약품안전청(FDA)은 Rebyota가 바이오매스 규정에 따라 엄격한 도우미 선별 및 제조 통제를 통과하여 안전과 품질 벤치 마크를 유지하고 있습니다. (출처: 미국 식품의약품안전처·
또한, 증가 임상 문제 (높은 반복률, 항생 저항 및 기존 치료의 제한된 효과와 같은) 재발생 감염에 의해 구성 된, 질병 통제 및 예방의 센터에 의해 underscored 것과 같은 의료 관련 감염의 광범위한 효과에 초점을 맞추고, 효과적인 비 항생제 개입에 대한 필요성을 높이화 - 약 1 약 31 명의 환자, 그리고 43 명의 간호 가정은 적어도 하나의 감염을 치료하는 동안. (출처: 질병 통제 및 예방 센터· 따라서,이 규제 명확성 및 강력한 임상 증거는 더 빠른 합격을 촉진하고 microbiome 치료 시장에서 Rebyota의 리더십 위치를 강화했습니다.
왜 Global Microbiome Therapeutics에서 가장 선호하는 행정 루트입니다 가격표 ·
이 보고서에 대해 자세히 알아보세요, 무료 샘플 다운로드
구두는 시장 점유율을 보유하기 위하여 계획됩니다 2.5% 할인 2026년에, 그것의 쉬운 참을성 있는 합격, 신청의 용이성 및 구두로 관리한 microbiome 처리를 위한 규제 지원을 증가합니다. 미국 FDA 승인 oral 살아있는 biotherapeutic 제품의 microbiome-containing 캡슐 (Vowst)와 같은, 위장 통로가 viable 박테리아를 위한 feasible 납품 경로 있다는 것을 보여줍니다. (출처: 미국 식품의약품안전처·
또한, 1 월 2026에서 Springer Nature Limited가 발표 한 연구는 microbiome 구두 치료가 내장 식물을 재분배하고 감염 재발을 방지 할 수 있음을 보여주었습니다. 실제로, 연구는 C. 항생 치료에 따라 difficile 감염에 대한 재발률이 환자의 20 ~ 30 %만큼 높을 수 있으므로 쉬운 솔루션 (출처 : 봄 자연 한정). simplicity의 이러한 요소, 향상된 접착율, 임상 효과는 microbiome therapeutics 시장에서 구강 관리에 대한 명확한 선호도를 주도했다.
병원 Segment 글로벌 Microbiome 치료 시장
병원 세그먼트는 시장 점유율을 보유하기 위해 계획된다 4.0% · 2026년에, 그것의 주요한 중요성 때문에 진보된 치료가 요구되는 복잡한 의학 케이스로 취급하기. 병원은 인간의 미생물을 사용하여 치료의 관리를위한 핵심 센터 역할을합니다. 또한 통제되는 조건 하에서 저장, 테스트 및 관리와 같은 생물학 제품의 관리를 위한 적절한 인프라를 제공합니다. 또한, 새로 승인 된 치료 및 병원 (Medicare, Medicaid 및 Diagnosis-Related Group (DRG) 지불 시스템)에 대한 reimbursement 정책의 증가 된 합격은 지배적 세그먼트를 만듭니다.
현재 이벤트와 영향력
현재 행사 | 묘사와 그것의 충격 |
산업 및 규제 푸시: Microbiome 치료제의 표준화 (2025) |
|
Biotherapeutic의 규제 진화 제품(Regulatory + Industry Shift, 2024–2025) |
|
75개 이상의 매개변수에 대해 검증된 매크로와 마이크로를 살펴보세요: 보고서에 즉시 액세스하기
(출처: Microbiome 치료 혁신 그룹· 미국 식품의약품안전처·
글로벌 Microbiome 치료 시장
이 보고서에 대해 자세히 알아보세요, 무료 샘플 다운로드
시장 드라이버
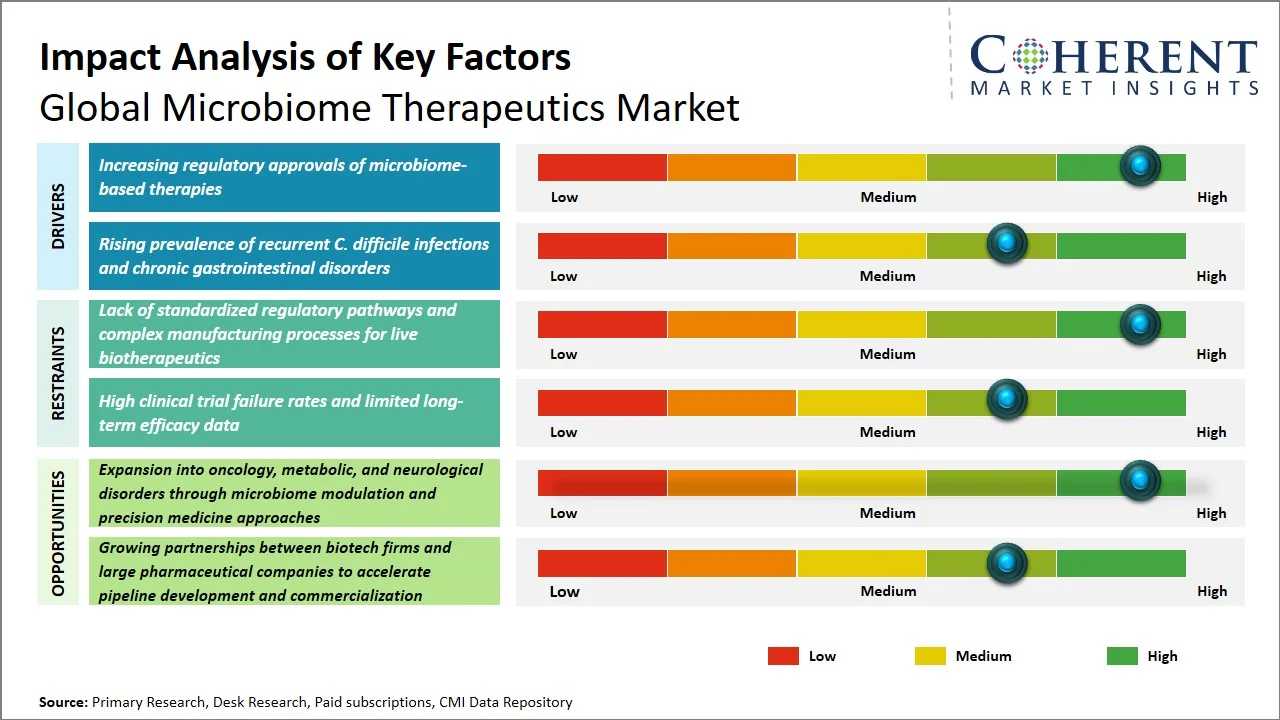
- microbiome 기반 치료의 규제 승인 증가 : S. FDA는 세계 최초의 구두 미생물 약물 인 Vowst를 승인하여 미생물 치료 시장 공간 (출처 : 미국 식품의약품안전처). 규제 승인은 연구 및 개발 활동에 투자를 늘리고 있으며 시장 성장에 기여했습니다. 또한, 그것은 연구 및 제품 개발 이니셔티브의 증가에 결과로 그들의 파이프라인을 개발하기 위해 투자자의 신뢰와 spurred 생물약학 기업을 개량했습니다. 따라서 규제 백킹은 microbiome 기반 치료 산업에서 상업화 및 혁신 프로세스를 가속화하는 데 사용됩니다.
- Recurrent C. difficile 감염과 만성 위장 장애의 상승:: 질병 통제와 예방 센터에 의해 보고된 것과 같이, C. diff는 미국에 있는 거의 절반 감염을 일으키는 것으로 추정됩니다. (출처: 질병 통제 및 예방 센터· 또한, 전임률은 2023년 각 100,000명 중 117.2 이상으로 추정되며, 질병의 지속적인 도전을 자극합니다. (출처: 질병 통제 및 예방 센터· 임상적 부담이 성장함에 따라 미생물 기반 치료의 사용을 중단하고, 이는 gut의 균형을 복원하고 기존 항생제에 더 나은 대안을 제공합니다.
Emerging 동향
- 이동 정밀도 Microbiome 치료: sequencing 기술 및 microbiome 분석의 사용은 특정 미생물을 기반으로 맞춤형 치료 프로그램을 설계 할 수 있습니다. 이 접근법은 암 및 대사 질병과 같은 조건을 위해 더 효과적인 치료 행정을 만들었습니다.
- 라이브 Biotherapeutic 제품 (LBPs)의 상승 초점: 기존의 Probiotics의 전환은 Live Biotherapeutic Products (LBPs)를 규제하는 Live Biotherapeutic Products (LBPs)가 미국 FDA와 같은 엔티티티의 임상 데이터 및 규제 승인에 의해 추진되는 순간을 얻고 있습니다. 따라서, 이 교대는 특정 의료 용도를 위해 설계되는 microbiome 근거한 치료의 발달을 보유합니다.
지역 통찰력
이 보고서에 대해 자세히 알아보세요, 무료 샘플 다운로드
왜 북미는 Microbiome 치료를위한 강력한 시장입니까?
북미는 세계 마이크로 바이옴 치료 시장을 선도, 추정에 대한 회계 0.5 %의 2026년, 항균성, 강한 임상 연구 생태계의 높은 prevalence로 빚어낸다. 질병 통제와 예방 센터에 따르면, 항균 저항은 미국에 있는 매년 2.8 백만개의 감염 그리고 약 35,000의 죽음을 일으키는 원인이 되고, 미생물에 근거를 둔 대체 처리 modality의 발달을 만들기. (출처: 질병 통제 및 예방 센터·
또한, 미생물 연구는 또한 인간적인 Microbiome 프로젝트와 같은 프로젝트를 통해 국가 보건 연구소에 의해 매우 촉진되고 인간적인 건강에 있는 미생물 역할로 종합적인 자료 세트 및 통찰력을 생성한 인간적인 건강에 있는 미생물 역할을, 가속하는 microbiome 근거한 치료 발달. (출처: 국립 보건 연구소· 중요한 의료 수요와 정부 지원 연구 프로그램의 존재는 시장 내의 지역 지배를 수립하는 데 도움이됩니다.
왜 아시아 태평양 Microbiome Therapeutics 시장 전시회 높은 성장?
Asia Pacific microbiome therapeutics 시장은 가장 빠른 성장을 전시할 것으로 예상됩니다. 25.5% 할인 2026년 글로벌 시장 점유율은 Clostridioides Difficile 감염, 위장 장애 및 대사 질환과 같은 감염을 포함하여 미생물 관련 질병에 대한 전임률의 높은 비율로 인해 발생합니다. 항생성, 중국, 일본, 한국 등 국가의 IBD의 경우와 같은 건강 문제의 증가로 인해 매우 높습니다.
또한, 아시아 태평양 지역의 microbiome 솔루션의 임상 개발 및 상용화에 대한 통합이되었습니다. 이것은 미생물에 대한 솔루션을 개발하기 위해 수행 된 바이오 기술 혁신 및 임상 연구의 증가 수에 의해 지원됩니다. 중국은 강력한 미생물 R & D 생태계를 설립했습니다. 또한, 일본은 제약 및 의료 기기법(PMD Act) 및 재생 의약품 안전법(ASRM) 규정을 통해 규제 승인을 얻기 위해 미생물과 관련된 제품을 쉽고 빠르게 만들어졌습니다.
글로벌 Microbiome 치료 시장 전망
왜 Microbiome Therapeutics 시장에서 혁신과 Adoption인가?
Microbiome 치료를위한 시장의 혁신과 채택은 강력한 임상 연구 인프라의 존재와 임상 시험의 높은 숫자로 인해 미국에 의해 떨어졌습니다. ClinicalTrials.gov에 제공된 정보에 따르면, 세계적으로 미국에 시행되는 microbiomes를 포함하는 임상 연구 시험의 실질적 번호가 다수 질병 표시 (출처: 임상시험.gov).
또한, 질병 통제 및 예방 센터는 표준 처리에 저항하는 감염의 일어나는 tide에 관하여 경보를 소리내어 입니다. 이 상황은 microbiome을 활용한 새로운 접근 방식에 대한 관심을 가져주고 있습니다. 지속적인 임상 연구와 새로운 해결책을 위한 누르는 필요 사이 명확한 연결은, 미국에서 microbiome 근거한 치료의 발달 그리고 합격을 가속화하는 차례로 입니다.
Microbiome Therapeutics Market에 대한 열정적인 시장은?
U.K.는 microbiome therapeutics, 강력한 규제 프레임 워크, 정교한 연구 인프라에 기여하고 새로운 치료 접근 방식에 중점을 둡니다. 의학 및 의료 제품 규제 기관 (MHRA)는 생물 공학 및 고급 치료를위한 잘 정의 된 통로를 제공하며 임상 개발 및 승인 프로세스를 간소화합니다.
또한 National Health Service (NHS)는 의료 배달 시스템 및 관련 자금 조달 메커니즘을 통해 혁신적인 치료의 통합을 촉진합니다. U.K. 또한 실질적인 정부 지원 연구 endeavors (U.K. Research and Innovation (UKRI), 건강 및 관리 연구 (NIHR) 및 Innovate UK)의 National Institute, 미국과 같은 엔티티티티티와 같은 혜택을 누릴 수 있습니다. 연구 및 혁신은 미생물과 생명 과학 연구에 대한 재정적 백업을 제공합니다. 따라서, 규제 투명성, 강력한 공공 의료 시스템 및 활성 연구 및 개발 지원의 확신은 미국을 미생물 치료를위한 유리하고 확장 시장으로 수립합니다.
중국 Microbiome Therapeutics 시장의 주요 성장 허브로 이수?
중국은 강력한 정부 지원, 활기찬 생명 공학 풍경 및 건강 문제의 상승 tide에 의해 추진 된 미생물 시장을위한 주요 성장 허브가 될 것으로 보인다. 예를 들어, 2023에서 중국은 합성 생물학 (61%), 게놈 sequencing 및 분석 (42%), 소설 항생제 및 항 바이러스제 (30%) 및 생물학 제조 (29%)을 포함하여 여러 생명 영역 과학 전반에 걸쳐 가장 인용 된 연구 논문에서 전 세계적으로 평가되었습니다. microbiome therapeutics의 발전을 직접 지원하는 강력한 연구 산출 및 혁신 용량을 강조합니다. (출처: 중국 연구의 Mercator Institute·
국가 보건위원회 (National Health Commission)를 통해 중국 정부는 생명 공학 및 정밀 의학을 미생물 연구의 우선 순위, spurring 혁신을 만들었습니다. 또한 중국 임상 연구 풍경은 microbiome-focused 연구 및 평가에서 눈에 띄는 증가와 더불어 급속하게 확장됩니다. 국가의 광대 한 환자 인구와 만성 및 대사 질환의 상승 인산은 또한 새로운 치료에 대한 수요를 밀어. 정책 지원의이 혼합, 연구 전진, 그리고 microbiome therapeutics를 위한 유망한 시장으로 중국 unmet 임상 필요 위치.
왜 독일은 유럽 Microbiome 치료 시장?
독일은 유럽 미생물 치료 시장이 강력한 바이오 기술 환경과 고급 의료 분야로 빚지고 있습니다. 국가는 약과 의료 기기의 연방 연구소의 존재에 의해 엄격한 규정을 즐긴다, 그로 인해 고급 치료의 연구 및 개발을 발전 돕는다. 또한, 국가는 연구 및 개발 활동을 위해 강력한 재정적 백업을 즐기고 미생물의 임상 연구에 적극적으로 참여합니다. 또한, 주요 제약 및 생명 공학 회사의 존재 (베이어 AG, BioNTech SE, Merck KGaA 및 Evotec SE와 같은) 속도 향상을 돕습니다.
프랑스의 Microbiome Therapeutics Market 개발은?
프랑스는 천천히하지만 확실히 microbiome 치료의 세계에서 강력한 선수가되고, 정부의 연구와 국가 프로그램에서 큰 파도에 의해 부유. 미생물 연구에 대한 제로 인 "프랑스 2030" 이니셔티브는 약 68.4 백만 달러 (€ 58 백만 달러)을 수료하여 미생물과 건강 사이의 링크로 깊은 연구에 의해 7 년 이상 연료 혁신에 도달하는 주요 예입니다. (출처: 프랑스 2030· 또한 프랑스 Gut 이니셔티브와 같은 야심 찬 프로젝트는 100,000 명에서 데이터를 수집하고, 프로세스에서 bolster 임상 연구. (출처: Microbiome 재단· 독일과 미국의 수준에서 아직은 아니지만 연구 시설의 증가 발전은 점차적으로 상승 시장으로 프랑스를 설립하고있다.
Global Microbiome Therapeutics Market에 준거한 조경
이름 * | 핵심 규칙 | 규제 개요 | 시장의 영향 |
북아메리카 | 미국 FDA - 라이브 바이오 치료 제품 (LBP) 가이드 라인; IND / BLA 경로 | Microbiome 치료는 통제됩니다 생명 공학IND 승인, 임상 시험 및 BLA 제출을 요구하는. FDA는 도우미 검열과 제조 통제를 포함하여 LBPs를 위한 특정한 지도를 제공합니다. | 높은 규제 의장은 안전과 효능을 보장합니다., 하지만 개발 타임 라인과 비용을 증가, 설립 된 선수 선호. |
유럽 연합 (EU) | 유럽 의학기구 (EMA); 고급 치료 약품 제품 (ATMP) 프레임 워크 | 관련 기사 생물학 약용 제품 및 ATMP중앙화된 승인을 요구하는. 품질, 안전 및 추적성에 대한 엄격한 지침은 시행됩니다. | Stringent 규정은 제품 신뢰성 향상, 그러나 입장 장벽 및 지연 상업화 창조하십시오. |
아시아 태평양 | PMDA (일본), NMPA (중국), CDSCO (인도) | 규제 프레임은 관련 기사, biologics와 cell/gene 치료 통로를 통해 정렬 증가. 일본은 재생 의학 법의 밑에 가속된 승인을 지원합니다. | 일부 국가의 패스너 승인 (예 : 일본) 구동 혁신, 규제 가변성은 시장 진입 문제를 만듭니다. |
라틴 아메리카 | ANVISA (브라질), COFEPRIS (멕시코) | 규정은 회사연혁, 종종 미국 / EU 프레임 워크를 참조. microbiome 치료를위한 승인 경로는 덜 정의됩니다. | Moderate 규제 장벽, 하지만 명확성의 부족은 느린 채택과 투자. |
중동 및 아프리카 | SAHPRA (남아프리카) | 규제 시스템 인기 있는, 크게 국제 기준 (FDA/EMA)에 기초를 두어. microbiome-specific 가이드라인 | 성장 시장 잠재력, 그러나 규제 불확실성 및 인프라 격차 제한 급속한 성장. |
75개 이상의 매개변수에 대해 검증된 매크로와 마이크로를 살펴보세요: 보고서에 즉시 액세스하기
microbiome modulation 및 Precision Medicine을 통해 oncology, metabolic 및 neurological 장애로 확장되는 방법은 글로벌 microbiome 치료 시장에서 새로운 성장 기회를 창출하는 것입니다?
암, 대사 문제 및 신경 질환을 치료하는 미생물의 사용은 개인화 된 의료를 허용하므로 고려 가능한 성장 기회를 제공합니다. 각 조건에 연결된 특정 미생물을 고려하여 특정 미생물을 고려하십시오. 세계 보건기구 (World Health Organization)에 따르면 약 20 만 개의 새로운 암 사례와 9.7 백만 개의 암 관련 사망자가 2022 년에 전 세계적으로보고되었습니다. 또한 암 진단이 5 년 이내에 살아남은 추정 된 사람들의 수는 53.5 백만, 소설 솔루션에 대한 필요성을 제안합니다. (출처: 세계 보건기구·
또한, 7 월 2023에 출판 된 국립 보건 연구소 (National Institutes of Health)에 의해 지원 된 연구는 미생물, 대사 및 신경질 장애 (출처 : 국립 보건 연구소). 건강 관리 설정의 microbiome의 중요성은 타겟팅 및 개인화 된 서비스를 제공하는 혁신을 선도 할 것입니다. microbiome 귀중한 치료 분야를 만드는.
시장 선수, 키 개발 및 경쟁 지능

이 보고서에 대해 자세히 알아보세요, 무료 샘플 다운로드
주요 개발
- 2월 2026일 Metagen 치료 닫힌 시리즈 B 펀딩 라운드, 약 23.8 백만 (JPY 3.5 억). 이 회사의 총 자본을 USD 36.7 백만 (JPY 5.4 억)에 가져, 일본에서 개발 된 gut microbiome 치료를위한 글로벌 임상 시험 속도를 높이기 위해 설계된 이동. 새로운 자금은 미생물 기반 약물 개발을 추진하고 회사의 임상 단계 파이프라인을 확장하는 데 도움이됩니다.
- 2월 2026일 팝업레이어 알림 Lishan Biotech는 BMC128 (LS-LBP-002)에 대한 라이센싱 거래를 위조했으며, 미생물 연구에 뿌리를 둔 암 치료 후보. 이 파트너십은 항 종양 면역 반응을 향상시키고 종양학 분야에서 미생물학의 발전을 가속화하도록 설계되었습니다.
공급 업체
microbiome therapeutics 시장은 현재 중요한 경쟁에 의해 표시되고, 둘 다 설치된 세계적인 약제 entities 및 nascent biotech 회사, 전문화한 치료의 발달에 강조하여 모든 propelled. 이 경쟁적인 환경은 기술적인 숙련도에 의해 크게 정의되고, 규제 기준에 고착하고, 비용 효과의 추적, microbiome 근거한 치료 접근에 있는 inherent 및 동적인 특성. 핵심 초점 지역은 다음을 포함합니다:
- Pipeline 확장 및 임상 시험 발전
- 전략적 협업 및 파트너십
- 규제 준수 및 품질 표준
- 고급 microbiome 플랫폼 개발 및 표적 치료
시장 보고서 Scope
Microbiome 치료 시장 보고서 적용
| 공지사항 | 이름 * | ||
|---|---|---|---|
| 기본 년: | 2025년 | 2026 년 시장 크기 : | 50-100 원 |
| 역사 자료: | 2020년에서 2024년 | 예측 기간: | 2026에서 2033 |
| 예상 기간 2026년에서 2033년 CAGR: | 3.6% 할인 | 2033년 가치 투상: | 50-100 원 |
| 덮는 Geographies: |
| ||
| 적용된 세그먼트: |
| ||
| 회사 포함: | Seres Therapeutics, Inc., Vedanta Biosciences, Inc., Finch Therapeutics Group, Inc., Enterome SA, 4D Pharma plc, Locus Biosciences, Inc., Rebiotix Inc., Second Genome Therapeutics, Microbiotica Ltd., 그리고 Synlogic, Inc. | ||
| 성장 운전사: |
| ||
| 변형 및 도전 : |
| ||
75개 이상의 매개변수에 대해 검증된 매크로와 마이크로를 살펴보세요: 보고서에 즉시 액세스하기
분석 Opinion (전문 Opinion)
- 미생물 기반 치료의 미래는 살아있는 생물 치료 제품 (LBPs)을 지원하는 새로운 증거에 의해 크게 영향을받습니다, 규제 지침의 변화, 그리고이 지역에 투자의 양. 정밀의학 및 생물학적을 향한 제약의 지속적인 동향으로 미생물은 실험적 치료 솔루션으로 전환합니다. 또한, 약물 개발, 생명 공학 회사 및 기타 개발 서비스 제공 업체의 아웃소싱 및 협업의 새로운 추세가 업계에서 중요한 역할을 할 것입니다.
- 시장 기회는 장 위장 질병 (GI), 특히 Clostridioides difficile 감염 (CDI) 및 종양학 및 면역학에 있는 그들의 사용을 위해 뜻깊은 것입니다. 미국을 위해, 성장은 호의를 베푸는 규제 풍경과 새로운 제품의 초기 승인과 함께 지원 규정의 존재로 인해 높은 것으로 예상됩니다. 중국을 위해, 성장은 microbiome 연구와 임상 프로그램의 발달에 있는 증가한 투자로 높은 것으로 예상됩니다.
- 경쟁자에 대한 이점을 얻기 위해, 그것은 늦은 단계 연구를 수행하여 임상 증명을 개발하는이 시장 집중에 선수가 생명의학의 확장 가능한 생산에 종사하고, 주요 제약 회사와 과학 기관과 협력을 창출하는 것이 필수적입니다. 또한, 규제 동향을 변경하고 신흥 시장 진입로가 중요합니다.
공유
저자 정보
Nikhilesh Ravindra Patel은 8년 이상의 컨설팅 경험을 가진 수석 컨설턴트입니다. 그는 시장 추정, 시장 통찰력, 트렌드 및 기회 식별에 능숙합니다. 시장 역학에 대한 깊은 이해와 성장 영역을 정확히 파악하는 능력은 그를 고객이 정보에 입각한 비즈니스 결정을 내릴 수 있도록 안내하는 데 귀중한 자산으로 만듭니다. 그는 보고서를 통해 시장 정보, 비즈니스 정보 및 경쟁 정보 서비스를 제공하는 데 중요한 역할을 합니다.
독점적인 트렌드 보고서로 전략을 혁신하세요:
자주 묻는 질문