グローバルマイクロバイオム治療薬市場規模と予測 - 2026 へ 2033
世界的なマイクロバイオオム治療市場は、成長することが期待されています ツイート 57.4 Mnの に 2026 へ 米ドル 310.6 Mn 2033年までに、化合物の年間成長率を登録 (CAGR)の 27.3%(税抜)お問い合わせ マイクロビオム治療薬の市場は、抗菌抵抗(AMR)の世界的な負担を増加させることで、大幅な拡大のために供給されます。
抗菌抵抗(AMR)が2021年の世界の推定4,71百万の死に、その1.14百万が抗菌抵抗(AMR)によって直接引き起こされたことを報告したLancetの調査。 Estimatesは、抗菌抵抗(AMR)による死亡率が2050年までに1億1億1千万に増加すると、総死亡率は8.22万に増加すると示唆しています。
(出典: ランセット)
また、世界銀行は、抗菌性(AMR)が2050年までの医療費1兆ドル、2030年までのUSD 1兆からUSD 3.4兆ドルまでの世界的なGDP損失が増加し、深刻な経済影響を強調したと推定しています。
(ソース): : : 世界銀行)
グローバルマイクロバイオメセラピューティクスマーケットの主要テイクアウト
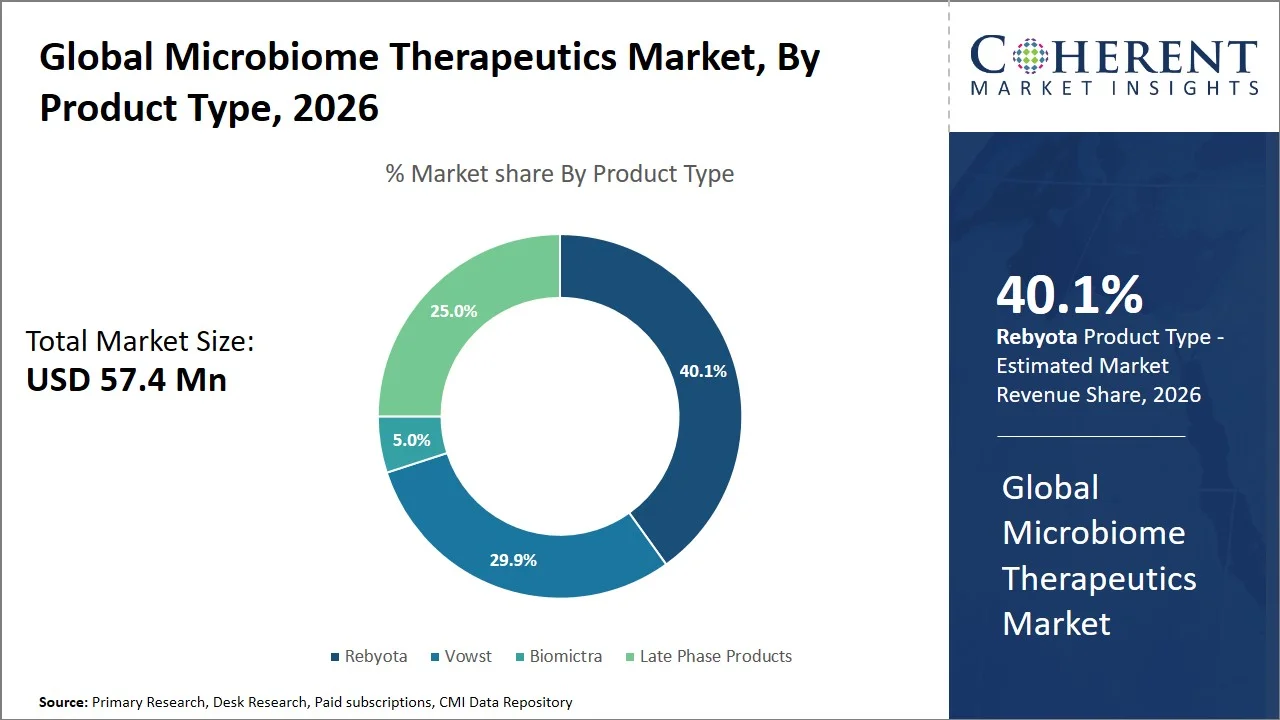
- Rebyota は、Rebyota を保有するプロジェクトです。 40.1の ツイート 2026年にグローバルマイクロバイオオム治療市場シェアのなかで、特に米国では、米国FDA承認の微生物薬および再発感染の治療における広範な使用として初めてのメリットを享受しています。 例えば、2022年11月、米国食品医薬品局は、フェリング医薬品の製品であるRebyotaにグリーンライトを与えた。 この承認は、米国で認可された最初のマイクロバイオオムベースの治療だったので、大幅でした。 薬は、抗生物質で処理された後、成人のクロステリジドの拡散性感染症のリターンを防ぐように設計されています。 (出典: 食品医薬品局)
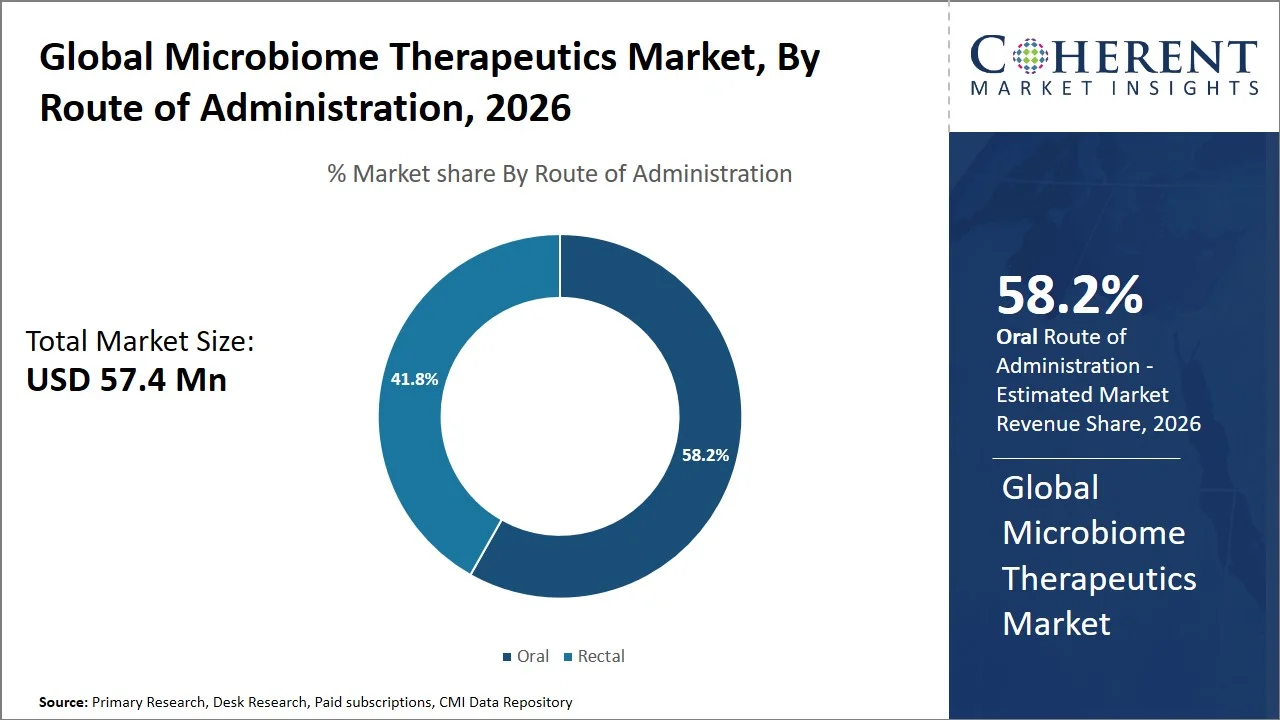
- オーラルは、 58.2マイル ツイート 2026年のグローバルマイクロバイオーム治療市場シェアで、管理セグメントの優位なルートを作る。 北米と欧州は、患者のコンプライアンス強化、非侵襲的なアプリケーションによる燃料供給、Vowstなどの経口微生物薬の承認数の増加により、セグメント内の重要な成長を目撃しています。 たとえば、Vowstを評価する臨床試験では、患者の成果や利便性が大幅に向上しました。 具体的には、Clostridioidesのdifficile感染の再発は、8週間のマークで39.8%と比較して、Vowstで約12.4%であった。 これは、経口、非侵襲的な投与方法により、強力な有効性とより良い患者の遵守を示す。 (出典: 食品医薬品局)
- 病院の区分は握るために写っています 47.0の ツイート 2026年のグローバルマイクロバイオオム治療市場シェアでは、医療施設の先進的なインフラ、最近発売されたバイオロジック、および臨床設定におけるマイクロバイオオムベースの治療薬の制御供給のための要件のために、北米でかなりの優位性を持つドミナンスを作る。 たとえば、マヨークリニックなどの専門医療および研究施設の拡大と、クリーブランドクリニックなどの施設で専用のマイクロバイオーム研究および治療プログラムの確立は、地域の強力な臨床インフラを強調しています。
- 北米は、予想されるシェアで優位性を維持 40. 40. 5%オフ 2026年に、主にマイクロバイオムベースの治療の早期規制承認、堅牢な研究努力、高度な生物学的治療の使用の増加による。 また、政府が支援する大規模なマイクロバイオムベースの研究活動とともに、堅牢な医療システムの可用性(例えば、ヒトマイクロバイオムプロジェクト)は、地域内での商業的な成功を促進するのに役立ちます。
- アジアパシフィックは、最も速い成長を期待し、予想される貢献を期待しています 22.(日) 5%オフ 2026年、バイオテクノロジーと精密医学に関する政府の重点強化、臨床試験の実施能力の増強、慢性疾患の患者の増加、規制インフラの進歩、ゲノムとマイクロバイオムの研究への資金の増大に伴い、シジブルな患者プールの共有。 たとえば、インドのゲノムインドプロジェクトでは、バイオテクノロジーの分野に裏打ちされた主要な精密薬が20以上の機関を結集しています。 全国ゲノムデータベースを作成するという目標で、10,000以上のゲノムサンプルを配列しました。 このデータベースは、高度な治療とマイクロバイオームの研究のためのリソースとして機能します。 (出典: Genome インド)
- アドジャンクトセラピーとしてのOncologyの拡張: : : 癌 免疫療法は、微生物治療薬が結果を改善する可能性がある領域としてます注目を得ています。 その結果、ニッチは、がん治療で使用されるチェックポイント阻害剤の有効性を高めることに重点を置いたコンビネーション療法内で登場しています。
- 経口カプセルベースのマイクロバイオムの開発 セラピス: 侵略からの移動 フェカル 標準的な経口カプセル配達への移植手順は、コンプライアンスとスケーリングを強化しています。 この開発は、収益性と便利なマイクロバイオムベースの薬のためのニッチ領域を作成しています。
なぜレビオタがグローバルマイクロバイオムの治療薬を支配するのか マーケット?
Rebyota は、市場シェアを保有するプロジェクトです。 40パーセント 2026年に、標準化された生体治療製品(LBP)として、確立された規制経路と臨床検証によって実証され、その後の微生物ベースの治療のためのモデルを確立しました。 米国食品医薬品局(FDA)は、Rebyotaは、生態学規制の対象であり、厳格なドーナースクリーニングと製造制御を網羅していることを示しています。これにより、安全性と品質のベンチマークが上昇します。 (出典: 米国食品医薬品局)
さらに、高再発率、抗生物質耐性、および従来の治療法の限られた有効性など、再発感染による増加する臨床的課題(高再発率、抗生物質耐性、および従来の治療法の限られた有効性など)は、病気のコントロールと予防のためのセンターが強調したため、医療補助感染の広範な効果に焦点を合わせ、効果的な非抗生物質介入の必要性が高まり、31人の入院患者で約1人、および43人の看護家庭で1人がケア中に少なくとも1人以上感染する。 (出典: 疾病予防センター) その結果、この規制の明快さと強力な臨床的証拠は、より迅速な受け入れを促進し、マイクロバイオーム治療市場でのRebyotaのリーダーシップポジションを強化しました。
グローバルマイクロバイオーム治療薬における行政の最優先ルート マーケット お問い合わせ
このレポートについてもっと知りたい方は, 無料サンプルをダウンロード
オーラルは、市場のシェアを保持するために投じられています 58.2%(税抜き) 2026年、患者の受け入れが容易で、適用の容易さおよび口頭管理されたmicrobiomeの処置のための調整可能なサポートを高めます。 米国FDAは、微生物汚染カプセル(Vowst)などの経口生体治療製品の承認を承認し、胃腸経路が生存可能な細菌のための可能な配送ルートであることを実証します。 (出典: 米国食品医薬品局)
さらに、2026年1月には、Springer Nature Limitedが公表した研究では、腸内細菌叢の再バランスと感染再発を防ぐことができることを臨床的に示しました。 実際、研究では、抗生物質療法後のC.の拡散率が患者の20〜30%高くなる可能性があることを示しています。したがって、簡単なソリューションの必要性(ソース: スプリング・ネイチャー・リミテッド)。 単純性、強化された付着率、および臨床的有効性のこれらの要因は、微生物治療市場で経口投与の明確な好みにつながります。
病院の区分は全体的な微生物療法の市場を支配します
病院の区分は市場の共有を握るために写っています 47.0%の 2026年に、高度療法が要求される複雑な医学の場合に対処することの彼らの主な重要性のために。 病院は、人間の微生物を使用して治療の管理のための重要なセンターとして機能します。 それらはまた制御された条件の下で貯蔵、テストおよび管理のような生物的プロダクトの管理のための十分なインフラを提供します。 また、新たに承認された療法の受入と、病院(メディケア、メディカエイド、および診断関連グループ(DRG)決済システム)に対する返金方針の改善が増加し、病院は優勢なセグメントを構成します。
現在のイベントとその影響
現在のイベント | 説明とその影響 |
業界・規制 プッシュ:マイクロビオム治療薬の標準化 (2025) |
|
ライブバイオセラピーの規制進化 製品(Regulatory + Industry Shift、2024–2025) |
|
75 以上のパラメータに基づいて検証されたマクロとミクロを発見: レポートにすぐにアクセス
(出典: マイクロバイオオム治療イノベーショングループ, 米国食品医薬品局)
グローバルマイクロバイオオム治療市場ダイナミクス
このレポートについてもっと知りたい方は, 無料サンプルをダウンロード
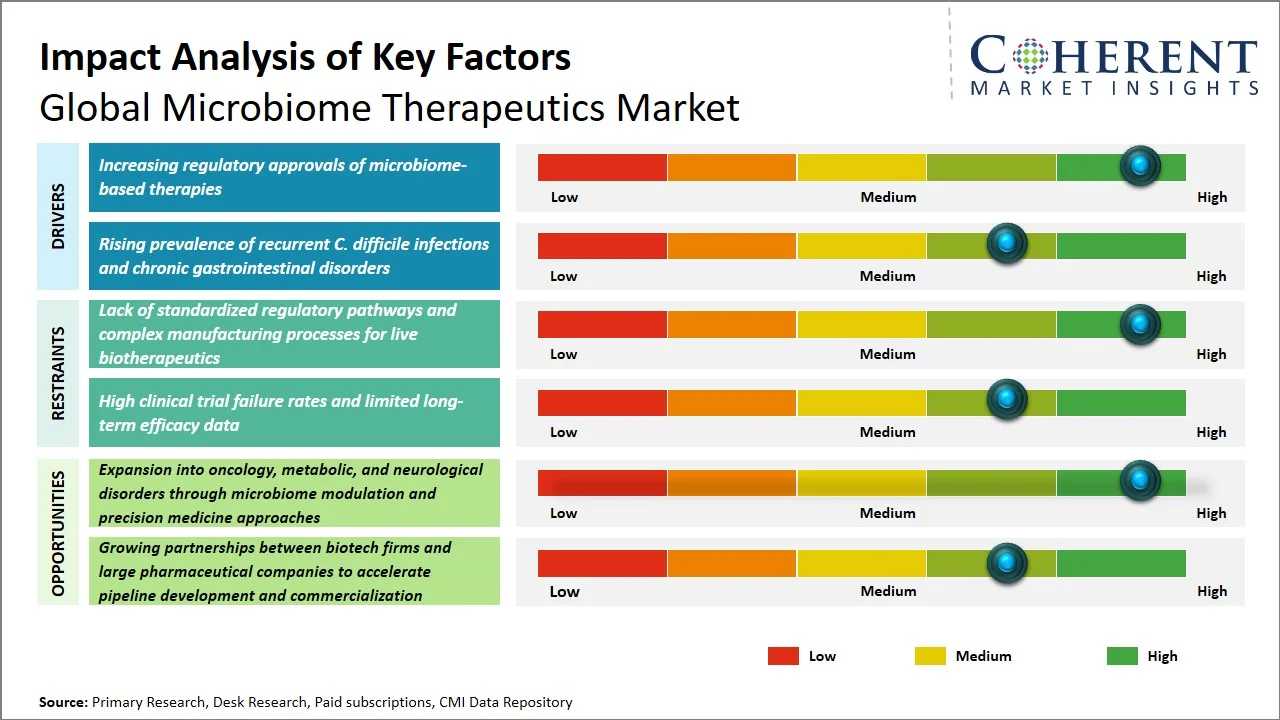
マーケットドライバー
- microbiomeベースの療法の規制承認の増加: S. FDAは、世界初の経口微生物薬、Vowstを承認しました。これは、マイクロバイオオム治療薬市場領域(出典: 米国食品医薬品局)。 規制当局の承認は、研究開発活動への投資の増加に役立ち、市場成長に貢献しました。 また、投資家の信頼度を高め、バイオ医薬品会社がパイプラインを開発し、臨床研究や製品開発の取り組みの増加を図っています。 したがって、規制裏付けは、マイクロバイオオムベースの治療業界における商品化と革新のプロセスをスピードアップして器械的になりました。
- 再発Cの有利な優先順位。 拡散感染と慢性消化管障害: : : 疾病予防センターが報告したように、C. diffは、毎年米国で約30万件の感染を引き起こすと推定されます。 (出典: 疾病予防センター) また、2023年に10万人以上から117.2以上と推定され、病気の継続的な課題を強調しています。 (出典: 疾病予防センター) 臨床的負担が増加するにつれて、マイクロバイオムベースの治療薬の使用が増加し、腸内のバランスを回復し、従来の抗生物質により良い代替手段を提供します。
新興トレンド
- 精密マイクロビオに向けてシフト セラピー: シーケンシング技術やマイクロビオム解析の使用は、個人固有のマイクロビオムに基づいてカスタマイズされた治療プログラムを設計することが可能になりました。 このアプローチは、癌や代謝疾患などの条件のために、より効果的、特に治療管理をしました。
- 生きている生物治療プロダクト(LBPs)の上昇の焦点: 従来のプロバイオティクスから規制された生体治療製品(LBP)への移行は、米国FDAのような企業から臨床データと規制の承認を蓄積することにより、運動量を増加させています。 その結果、このシフトは、特定の医療用途のために設計されているマイクロバイオオムベースの治療薬の開発を続けています。
地域洞察
このレポートについてもっと知りたい方は, 無料サンプルをダウンロード
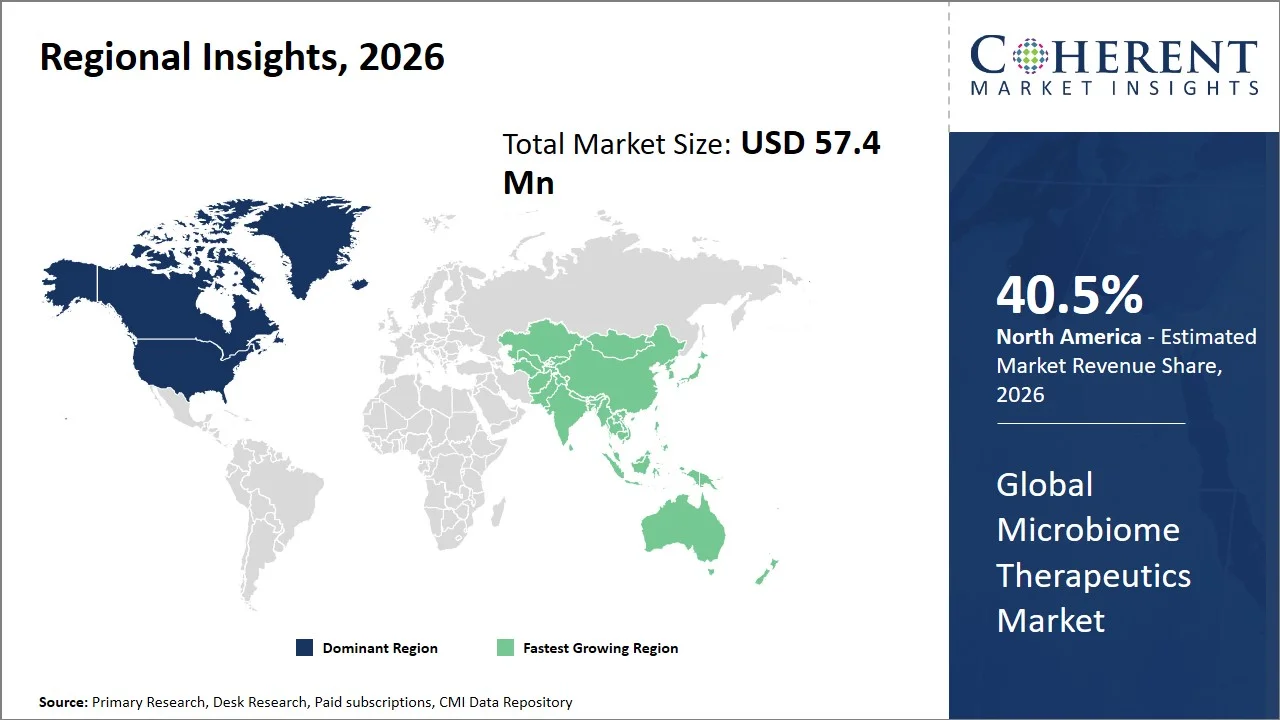
なぜ北アメリカがマイクロバイオムの治療薬の強い市場ですか?
北アメリカは推定のための会計処理の全体的な微生物治療の市場を導きます 40.5%の 2026年に分かち合い、抗菌性、強靭な臨床研究のエコシステムの高い優先順位を上げました。 疾病予防センターによると、抗菌抵抗は、毎年約2.8万人の感染症を引き起こし、米国だけでは年間約35,000回の死亡で、マイクロバイオムに基づく代替治療方法の開発を行っています。 (出典: 疾病予防センター)
また、微生物に関する研究は、ヒトマイクロバイオオムプロジェクトなどのプロジェクトを通じて、国立衛生研究所が推進するだけでなく、ヒトの健康における微生物の役割に関する包括的なデータセットやインサイトを生成し、マイクロバイオオムベースの治療の開発を加速しています。 (出典: 国立健康研究所) 重要な医療需要と政府支援の研究プログラムの両立は、市場での領域の優位性を確立するのに役立ちます。
アジアパシフィックマイクロバイオーム・セラピューティクス・マーケットはなぜ高成長?
アジア・パシフィック・マイクロバイオーム・セラピューティクス・マーケットは、最も速い成長を期待し、 22.5% 2026年のグローバル市場へのシェア, マイクロバイオオム・アソシエーション疾患の予防接種率が高いため, Clostridioides Difficile感染などの感染症, 消化管障害, 代謝疾患. 抗生物質耐性などの健康問題の増大に伴い、中国、日本、韓国などの国におけるIBD症例はかなり高い。
また、アジア太平洋地域におけるマイクロバイオムソリューションの臨床開発・商品化に向けた取り組みも行っています。 これは、微生物に関するソリューションを開発するために実施されているバイオテクノロジーの革新と臨床研究の増加の数でサポートされています。 中国は、強力なマイクロバイオム研究開発エコシステムを確立しました。 また、医薬品・医療機器法(PMD法)及び再生医療安全法(ASRM)法による規制承認を得るため、マイクロバイオオムを含む製品に対して、日本はより簡単かつ迅速に対応しています。
主要国のためのグローバルマイクロバイオオム治療市場見通し
なぜ、マイクロバイオーム治療市場における米国のリーディングイノベーションと採用は?
マイクロビオム治療薬の市場でのイノベーションと採用は、堅牢な臨床研究基盤の存在と高い臨床試験の進行状況のために、米国によって急上昇しています。 臨床Trials.govで提供されている情報によると、米国で行われる微生物叢を含む臨床研究試験のかなりの数があります。複数の病気の徴候に積極的な研究があることを示す(出典: 臨床トライアル.gov)。
また、疾病予防センターは、標準治療に耐性のある感染の上昇潮の警報を鳴らしています。 この状況は、マイクロバイオームを活用する人々を含む、新しいアプローチに興味を燃やしています。 継続的な臨床研究と新しいソリューションのプレスの必要性間の明確な接続は、順番に、米国のマイクロバイオオムベースの治療の開発と受け入れをスピードアップします。
U.Kは、マイクロバイオーム治療市場向けの好ましい市場ですか?
U.K.は、その堅牢な規制枠組み、洗練された研究インフラ、新たな治療アプローチに重点を置いた、マイクロバイオーム治療薬の推進環境を提示します。 医薬品およびヘルスケア製品規制庁(MHRA)は、臨床開発と承認プロセスを合理化することにより、バイオロジカルと高度な治療のための定義された経路を提供しています。
また、国立保健サービス(NHS)は、医療デリバリーシステムおよび関連する資金メカニズムを通じて、革新的な治療の統合を推進しています。 U.K.は、大幅な政府支援の研究活動(英国研究イノベーション(UKRI)、国立保健福祉研究所(NIHR)、英国イノベーターなど)の恩恵を受けています。 マイクロバイオームとライフサイエンスの研究のための財務支援 その結果、規制の透明性、強固な公衆医療システム、および積極的な研究開発支援のこの告白は、マイクロバイオーム治療薬の有利かつ拡大市場として英国を設立します。
中国は、マイクロバイオーム治療市場の主要な成長ハブとして新興していますか?
中国は、強力な政府サポート、活気あるバイオテクノロジーの風景、そして健康課題の上昇潮流によって推進される微生物治療市場のための主要な成長ハブであるように見えます。 たとえば、中国は2023年に合成生物学(61%)、ゲノムシーケンシングおよび分析(42%)、新規抗生物質および抗ウイルス(30%)、および生物学的製造(29%)を含む複数のライフサイエンス領域にわたって最も引用された研究論文で世界初にランクされています。 (出典: 中国研究の水力学研究所)
中国政府は、国家衛生委員会を通じて、バイオテクノロジーと精密医学を優先し、マイクロバイオーム研究におけるイノベーションを浄化しました。 さらに、中国の臨床研究の風景は急速に拡大し、マイクロバイオムに焦点を当てた研究と試験の顕著な増加が増加しています。 国の広大な患者集団と慢性および代謝疾患の上昇の発生率は、新しい治療法の需要を高めています。 政策サポート、研究の進歩、および非メートルの臨床必要性のこのブレンドはマイクロバイオムの治療薬のための有望な市場として中国を置きます。
なぜドイツはヨーロッパマイクロバイオム治療市場をトップにしていますか?
ドイツは、その堅牢なバイオテクノロジー環境と高度な医療分野へのヨーロッパマイクロバイオーム治療市場を支持しています。 国は、医薬品および医療機器の連邦研究所の存在の影響を受け、厳しい規制を楽しんでいます。これにより、先進的な治療法の研究と開発を進めることができます。 また、研究・開発活動に強い金融裏付けを行い、微生物の臨床研究に積極的に参加しています。 また、主要な医薬品・バイオテクノロジー企業(バイエルAG、バイオNTech SE、メルクKGaA、エボテックSEなど)の存在により、高度化が図れます。
フランスのマイクロバイオオム治療薬市場は発展していますか?
フランスは、マイクロバイオム治療薬の世界では、確かに強い選手になりつつありますが、政府の有益研究と国家プログラムのサージによってbuoyed。 マイクロバイオーム研究でゼロになる「France 2030」の取り組みは、マイクロバイオームと健康の間のリンクに深く掘り下げることで、7年以上にわたり、約68.4億米ドル(約58万ユーロ)のチャネルで重要な例です。 (出典: フランス 2030) さらに、フランスのグットイニシアチブのような野心的なプロジェクトは、100,000人からデータを収集し、プロセスでは、臨床研究を強化することを目指しています。 (出典: マイクロバイオム財団) ドイツと米国ではまだないが、研究施設の増大発展は、上昇市場としてフランスを徐々に確立しています。
グローバルマイクロバイオム治療市場を統治する規制風景
地域紹介 | 主な規制 | 規制の概要 | 市場への影響 |
北アメリカ | 米国FDA – 生体治療製品 (LBP) ガイドライン; IND/BLA 経路 | マイクロビオム治療薬は、 バイオロジックIND の承認、臨床試験、および BLA の提出を要求する。 FDAは、ドナースクリーニングおよび製造制御を含むLBPの特定のガイダンスを提供します。 | 高い規制の厳格さは安全および効力を保障します, しかし、開発のタイムラインとコストを増加, 確立された選手を支持. |
ヨーロッパ | 欧州医薬品庁(EMA)、高度治療薬製品(ATMP)フレームワーク | 規制下 生物医学プロダクトおよびATMPs、集中された承認を要求します。 品質、安全性、トレーサビリティに関する厳格なガイドラインが施行されています。 | 厳しい規則により製品の信頼性が向上、しかし記入項目の障壁を作成し、商品化を遅らせて下さい。 |
アジアパシフィック | PMDA(日本)、NMPA(中国)、CDSCO(インド) | 規制フレームワークは 進化するバイオロジックとセル/遺伝子治療経路へのアライメントの増加 日本では、再生医療法に基づく早期承認をサポートしています。 | 一部の国における迅速な承認(例:日本) 規制の分散性が市場参入の課題を創出しながら、イノベーションを推進します。 |
ラテンアメリカ | ANビザ(ブラジル)、COFEPRIS(メキシコ) | 規制は 研究開発米国/EUフレームワークを参照することが多い。 マイクロビオム療法の承認経路は定義されていないままです。 | モデレート規制の障壁、しかし明快さの欠如は採用および投資を遅らせるかもしれません。 |
中東・アフリカ | SFDA(サウジアラビア)、SAHPRA(南アフリカ) | 規制制度はあります 新規参入、国際規格(FDA/EMA)に基づいて主に。 マイクロバイオム固有のガイドラインを限定。 | 市場の潜在的な成長, しかし、規制の不確実性とインフラギャップは、急速な成長を制限します. |
75 以上のパラメータに基づいて検証されたマクロとミクロを発見: レポートにすぐにアクセス
微生物変調と精密医学による腫瘍学、代謝、神経障害の拡大は、世界的な微生物治療市場で新しい成長機会を作成する方法?
マイクロバイオオムの治療薬を使用して、がん、代謝の問題、および神経障害を治療することは、各条件にリンクされている特定の微生物を考慮に入れ、パーソナライズされた医療を可能にするため、かなりの成長機会を提供します。 世界保健機関によると、2022年に世界規模で約200万人の新がん症例と、約97万人のがん関連死亡が報告されました。 また、がん診断後5年以内に生きた人の推定数が53.5万件で、新規ソリューションの必要性を示唆しています。 (出典: 世界保健機関)
さらに、2023年7月に公表された国立衛生研究所が支持する研究では、マイクロバイオオムは免疫反応、代謝経路、神経系(腸内脳軸)を腫瘍学的、代謝、神経障害(出典: 国立健康研究所)。 ヘルスケア設定におけるマイクロビオムの重要性は、ターゲットとパーソナライズされた治療サービスを提供する革新につながるでしょう。
市場プレーヤー、キー開発、および競争力のあるインテリジェンス

このレポートについてもっと知りたい方は, 無料サンプルをダウンロード
主な開発
- 2月2026日 メタゲン治療薬 シリーズを閉じる B 資金調達ラウンド、約 23.8 百万米ドル (3.5 億円) 同社の総資本金をUSD36.7億米ドル(5.4億円)に増資し、日本で開発された腸内微生物治療薬の世界的な臨床試験をスピードアップする。 新しい資金は、微生物ベースの医薬品の開発を推進し、同社の臨床段階パイプラインを拡大するのに役立ちます。
- 2月2026日 エボジェネ株式会社 そしてLishan Biotechは、微生物研究に根ざしたがん治療候補であるBMC128(LS-LBP-002)に関するライセンス契約を造りました。 このパートナーシップは、腫瘍学の分野における微生物治療の進歩を促進し、抗腫瘍免疫反応を高めるように設計されています。
競争力のある風景
マイクロバイオオム治療市場は、現在重要な競争によってマークされています, 確立されたグローバル製薬企業とナスセントバイオテクノロジー企業の両方を網羅, 専門療法の開発に重点を置いたすべての. この競争環境は、技術的能力によって主に定義され、規制基準に準拠し、コスト効率性を追求し、マイクロバイオオムベースの治療アプローチに固有の複雑で動的特性をミラーリングします。 主な焦点区域は下記のものを含んでいます:
- パイプラインの拡張と臨床試験の進歩
- 戦略的コラボレーションとパートナーシップ
- 規制遵守と品質基準
- 高度なマイクロバイオムプラットフォームの開発と標的療法
マーケットレポートスコープ
マイクロバイオオム治療薬市場レポートカバレッジ
| レポートカバレッジ | ニュース | ||
|---|---|---|---|
| 基礎年: | 2025年 | 2026年の市場規模: | 米ドル 57.4 Mn |
| 履歴データ: | 2020年~2024年 | 予測期間: | 2026 へ 2033 |
| 予測期間 2026〜2033 CAGR: | 27.3%(税抜) | 2033年 価値の投射: | 米ドル 310.6 Mn |
| 覆われる幾何学: |
| ||
| カバーされる区分: |
| ||
| 対象会社: | セレス・セラピューティクス株式会社、ヴェーダンタ・バイオサイエンス株式会社、フィンチ・セラピューティクス・グループ株式会社、エンタメ・SA、4Dファーマ、ローカス・バイオサイエンス株式会社、レビオチックス株式会社、セカンド・ゲノム・セラピューティクス、マイクロバイオティクス株式会社、シンロジック株式会社 | ||
| 成長の運転者: |
| ||
| 拘束と挑戦: |
| ||
75 以上のパラメータに基づいて検証されたマクロとミクロを発見: レポートにすぐにアクセス
アナリストオピニオン(エキスパートオピニオン)
- マイクロバイオオムベースの療法の将来は、生体治療製品(LBP)、規制ガイドラインの変更、およびこの分野への投資の量をサポートする新しい証拠によって大きく影響されます。 精密医薬品や生物学への医薬品のトレンドが続く中、微生物治療薬は実験から商品化まで移行します。 また、医薬品開発、バイオテクノロジー企業、その他の開発サービスプロバイダにおけるアウトソーシングとコラボレーションの新たなトレンドが業界内で重要な役割を果たします。
- 市場機会は、消化管の病気(GI)、特にClostridioidesのdifficileの伝染(CDI)および腫瘍学および免疫学のそれらの使用のために重要なです。 米国では、有利な規制の景観と支持規則の存在により、新製品の早期承認による成長が高まることが期待されています。 中国では、微生物の研究開発や臨床プログラムの開発における増加した投資により、成長が高まることが期待されます。
- 競合他社に優位性をもたらすために、この市場でのプレイヤーは、生体治療薬のスケーラブルな生産に取り組み、主要な製薬会社や科学機関とのコラボレーションを創出することにより、臨床証拠の開発に集中することが不可欠です。 また、規制動向の変化に精通し、新興市場参入が重要となります。
著者について
Nikhilesh Ravindra Patel は、8 年以上のコンサルティング経験を持つシニア コンサルタントです。市場予測、市場インサイト、トレンドと機会の特定に優れています。市場動向に対する深い理解と成長分野を正確に特定する能力により、情報に基づいたビジネス上の意思決定をクライアントに導く上で、彼は非常に貴重な存在となっています。レポートを通じて、市場情報、ビジネス情報、競合情報サービスを提供する上で重要な役割を果たしています。
独占トレンドレポートで戦略を変革:
よくある質問