第一次胆管支炎の処置の市場のサイズおよび予測
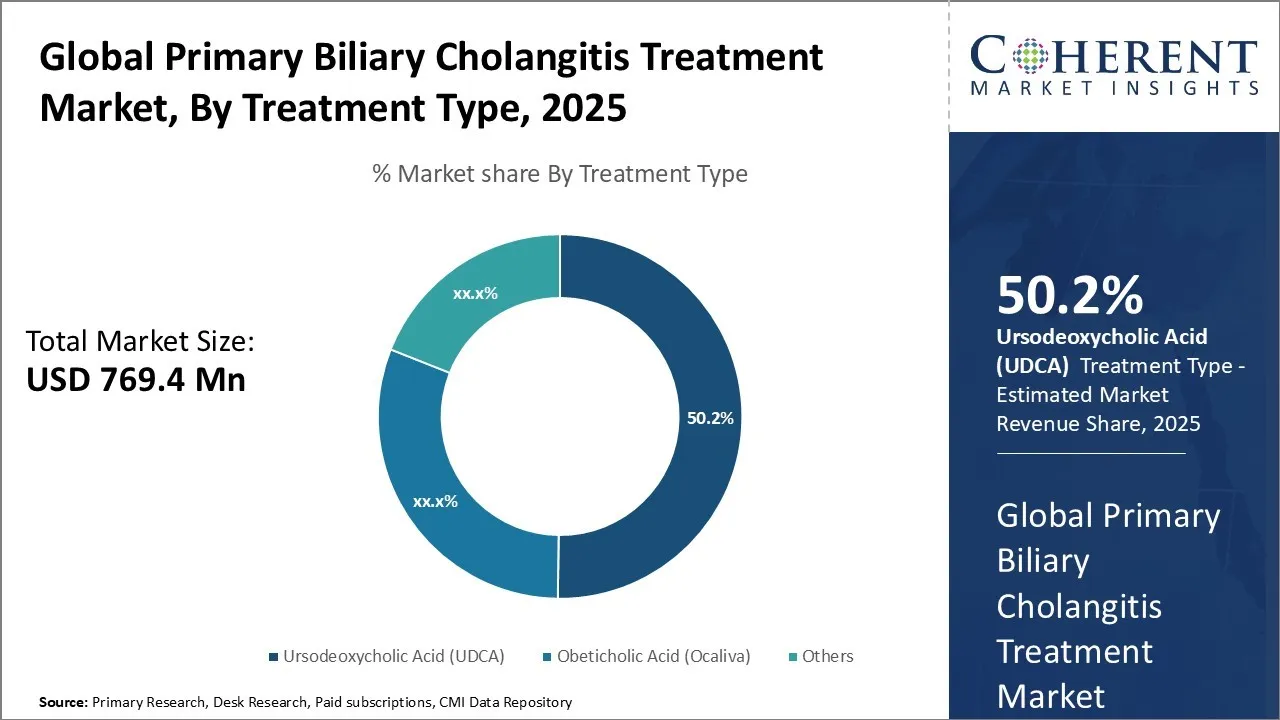
第一次性胆管支炎の処置の市場のサイズは評価されると推定されます 米ドル 769.4 Mn 2025年、到達見込み 米ドル 1,388.5 Mn 2032年、化合物の年間成長率を展示 (CAGR) 8.8%2025年~2032年
キーテイクアウト
- 治療の種類に基づいて、ウルゾデオキシコール酸(UDCA)セグメントは、プライマリ胆管支炎の最初のライン治療であるため、2025年に市場で最も高いシェアをキャプチャすることが期待されています。
- 分布に基づく チャネル、病院の薬局の区分は専門家によって規定される薬物を提供する機能による2025の市場の彼最大のシェアを捕獲するために写っています。
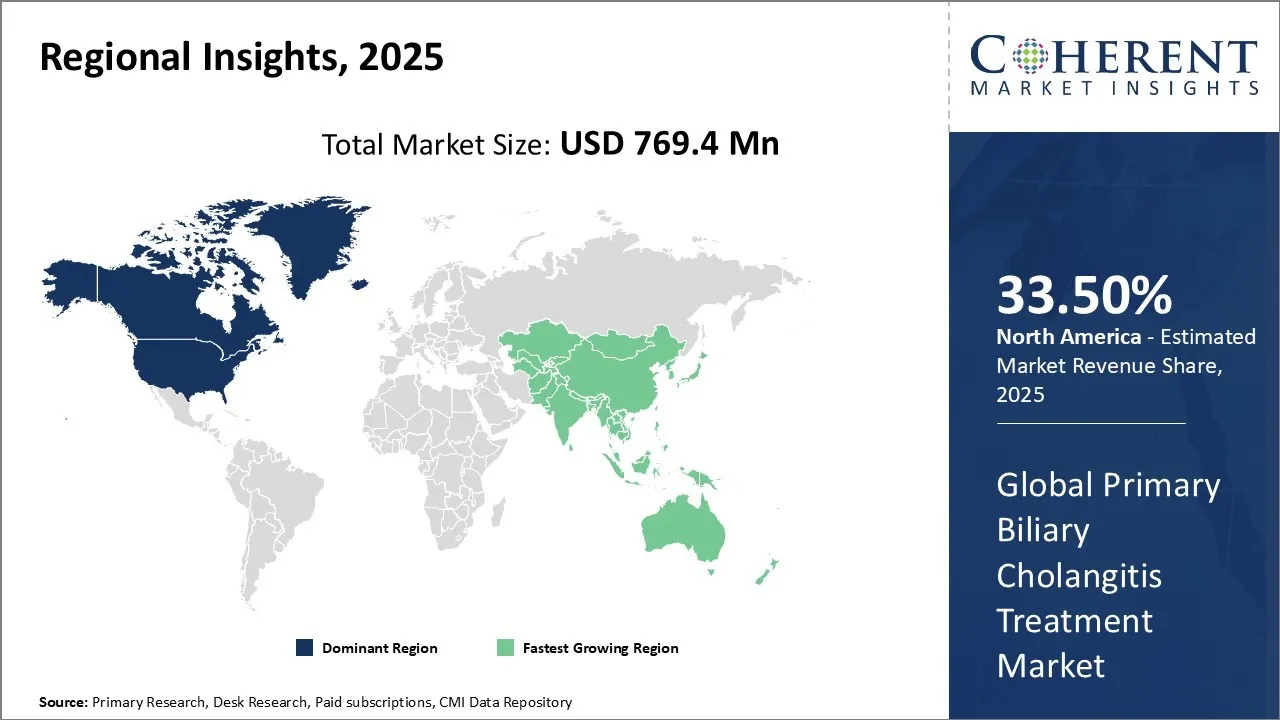
- 地域に基づいて、北アメリカは2025年に世界一次胆管支炎の処置の市場を、33.5%のシェアと導くために置きます。 欧州は予測期間中に最も急速に成長する地域になることを期待しています。
市場概観
第一次性胆嚢炎 治療市場需要は、高まる診断速度、非メートルの臨床ニーズ、および新しい薬物承認のために着実に成長しています。 希少疾患の調査、アクセスの改善、規制機関からの支援に重点を置き、市場拡大を促す。
初期の段階ではPBCの症状がない人が多い。 病気が進行するにつれて、胆道疾患の徴候が現れ始めます。 PBCを持つ人々の最も初期と最も一般的な症状は、疲労とかゆみの皮膚です。 これらの症状は、異なる程度に異なる人々に影響を与えます。 彼らは病気の経過で後でまたは早期に起こることができ、そして彼らはどんな段階でも軽度にすることができます。
現在のイベントとその主な胆管支炎治療市場への影響
現在のイベント | 説明とその影響 |
アメリカ PBC療法に関する規制決定 |
|
臨床パイプラインの開発 |
|
75 以上のパラメータに基づいて検証されたマクロとミクロを発見: レポートにすぐにアクセス
返金ポリシー
第一次性胆管支炎(PBC)治療のための払い戻し方針は、ヘルスケアシステム構造と薬物承認状況によって形作られた、世界的な市場で著しく変化します。 米国では、URsodeoxycholic 酸 (UDCA) や obeticholic 酸 (Ocaliva®) などの治療は Medicare および私的保険の下で再燃されますが、事前の承認とステップ療法が一般的です。 ヨーロッパでは、国家保健システムがUDCAのような第一線療法をカバーしていますが、第二線治療はしばしば遅延または条件付き払い戻しに直面しています。 たとえば、英国では、NICE は NHS のリミューズメントの elafibranor (Iqirvo®) を 2 行目のオプションとして承認しました。 ドイツとフランスは、通常、法的な保険の下でより広いアクセスを提供していますが、費用対効果の高いレビューを課す可能性があります。 日本では、国民保険制度に基づくPBC治療をカバーしていますが、厳格に含める基準が適用される場合があります。 ブラジルやインドなどの新興市場は、公正な払い戻しが限られており、患者は、多くの場合、預言者の支払いや民間のカバレッジに依存しています。 グローバルに、アクセスと手頃な価格は、直接健康当局鑑定に結び付けられ、費用対効果と臨床的利益は、償還決定における重要な決定要因となります。
第一次胆管支炎の処置の市場洞察、処置のタイプによる
Ursodeoxycholicの酸(UDCA)の区分は全体市場を支配します
治療タイプでは、尿素酸(UDCA)は、ほとんどのPBC患者のための最初のライン標準療法であり、疾患の進行を遅くし、肝酵素レベルを改善する効果のために10年間にわたって広く使用されているので、2025年に市場で最大のシェアを保持することが期待されています。 Ursodeoxycholicの酸はOcalivaの酸(Ocaliva)およびfibratesとの比較で広く利用でき、現実的です、特に初期病期の。
2024年12月、CDSCOの被験者委員会は、Abbottヘルスケアの承認を付与し、尿道酸(UDCA)錠剤(300mgおよび450mg)を製造し、産後コレステロール症の治療、妊娠中の潜在的に深刻な肝臓状態を承認しました。 決定は、臨床データの包括的な見直しに従い、委員会は3ヶ月以内に提出するプロトコルで、市販の監視研究を管理しました。 UDCAは、胆汁の流れを改善し、肝細胞を保護し、重度のかゆみからの救済を提供し、母親と胎児の両方にリスクを減らすことによって動作します。 Abbotのエントリは、インドで治療オプションを広げることが期待されます。
第一次性胆嚢炎の処置の市場洞察、配分チャネルによる
病院薬局は、その専門処方薬を借りています
分配チャネルの面では、病院の薬剤師の区分は2025年の市場の最も高い共有に貢献し、尿道酸、obeticholic酸のような専門にされた規定された薬物を提供する能力にowing期待されます。これはより一般的に開始され、病院の設定で分配されます。 PBCの承認または調査薬は通常、管理プロトコルおよび監視ニーズによる病院および専門薬局を通じて配布されます。
米国各地の病院は、第一次胆管支炎(PBC)のための2つの新しくFDA承認経口薬を貯蔵し始めています。 IpsenのIqirvo (elafibranor)は6月にUrsodeoxycholicの酸(UDCA)またはUDCA-intolerantの患者のmonotherapyの使用のための加速された承認、demonstrating減らされたアルカリのリンカゼおよびかゆみの軽減を受け取りました。 例えば、2024年8月には、GileadのLivdelzi(seladelpar)がFDAのクリアランスを受け取り、UDCAの不十分な応答で強力な生化学的反応とpruritusの改善を示す。 主要な病院の処方に含まれていると、これらのエージェントは、米国で約100,000人の成人に影響を与えるPBCを管理するための臨床医の新しい選択肢を提供しています。
地域洞察
このレポートについてもっと知りたい方は, 無料サンプルをダウンロード
北アメリカの第一次性胆嚢炎の処置の市場分析及び傾向
北米地域は、2025年の33.50%のシェアで市場をリードする予定です。 米国とカナダを含む地域は、十分に確立された医療インフラを持ち、Intercept Pharmaceuticals, Inc.、GSK plc.、Bristol-Myers Squibb and Company、Enanta Pharmaceuticalsなどの主要なプレーヤーの強力な存在を持っています。 北米における第一次胆管支炎治療の市場は、増加の研究と開発活動によって駆動され、重要であると予想されます。 例えば、2025年11月には、医薬品のインターセプト、 バイオ医薬品 企業は、第一次胆管支炎(PBC)の患者のための結果を改善するために、肥満酸(OCA)の可能性を評価する2つの分析の結果を発表しました。
ヨーロッパ第一次性胆嚢炎治療市場分析と傾向
欧州地域は、予測期間中に市場で最速の成長を期待しています。 ヨーロッパ地域はPBCの新しい治療薬の開発に強い焦点を合わせています。 ドイツ、フランス、英国などの国々は、PBCの医薬品の需要に寄与する堅牢なヘルスケア製薬会社を持っています。 ヨーロッパの市場は、プライマリ胆管支炎(PBC)の増大による安定した成長を経験することが期待されています。 例えば、2025年2月、欧州委員会は、プライマリ・バイリー・カランヒュア(PBC)の治療として、尿道酸化塩酸を成人に不十分な応答で補完または交換するスラデルパー(Livdelzi)を承認しました。 決定は、責任試験に基づいてCHMP肯定的な意見に従い、アルカリリンガターゼおよびプルリタスの改善を実証します。
第一次性胆管支炎の処置の市場展望の国-Wise
米国第一次胆管支炎治療市場動向
米国第一次胆管支炎の処置の市場は上昇のprevalenceおよび早い診断によって特徴付けられます。 国立衛生研究所によると、PBCは、より優れた診断意識と肝機能スクリーニングテストの拡張使用のために、米国で40歳以上1,000人の女性に推定1に影響を与えます。 U.S.患者は、尿素酸(UDCA)や、ホウ酸(Ocaliva)などの承認療法にアクセスし、病院と専門薬局の両方で広く入手可能です。 PBCers Organization や American Liver Foundation などの組織の患者様によるさらなる移動、強固な予防接種により、教育、早期テスト、サポート、診断および治療の取り込みを促進します。 これは、プライマリ胆管支炎市場シェアをさらに増殖します。
U.K. 第一次胆嚢炎治療市場動向
U.K. 第一次胆管支炎治療市場は急速に拡大しています, 高アンメット医療ニーズを含むPBCの拡張処理オプションによって燃料を供給, 矛盾し、標準ケアと多く. 患者の約40%は、第1線治療(UDCA)に完全対応せず、第2線治療には30%以上対応できません。 効果的な選択肢がなければ、病気の進行は肝臓の故障と移植につながることができます。 NHS病院を覆う国家監査は、UDCA投薬、症状監視、移植評価の広範囲にわたる不足が見られます。 PBCは、主に中高齢の女性である英国で約20,000〜25,000人の人々に影響を与え、移植や合併症に関連する生活の質とNHSコストに大きな影響を与えます。
マーケットレポートスコープ
第一次性胆管支炎の処置の市場報告の適用範囲
| レポートカバレッジ | ニュース | ||
|---|---|---|---|
| 基礎年: | 2024年(2024年) | 2025年の市場規模: | 米ドル 769.4 Mn |
| 履歴データ: | 2020年~2024年 | 予測期間: | 2025 へ 2032 |
| 予測期間 2025〜2032 CAGR: | 8.8% | 2032年 価値の投射: | 米ドル 1,388.5 Mn |
| 覆われる幾何学: |
| ||
| カバーされる区分: |
| ||
| 対象会社: | インターセプト医薬品、ハイライト治療薬、S.L.、GSK plc。、ブリストル・マイアス・スクイブ、エンタット・ファーマ、NWバイオ医薬品、メルク&Co株式会社、Ipsenファーマ、ジョンソン&ジョンソン、GENFIT、アイアンウッド・ファーマ、Inc.、ノバルティス、COURファーマ、Ken Pharmaceutical Co.、株式会社。 | ||
| 成長の運転者: |
| ||
| 拘束と挑戦: |
| ||
75 以上のパラメータに基づいて検証されたマクロとミクロを発見: レポートにすぐにアクセス
第一次胆管支炎の処置の市場運転者
- 第一次性胆管支炎の増大の可能性:世界的な第一次胆道胆道炎の治療市場の成長を燃やす主要な要因の1つです。 ライフスタイルの変化と寿命の延伸、肝疾患は効果的な治療オプションを必要とする上昇にあります。 第一次胆道角膜炎治療は、このような複雑な病気を治療するために、より標的と効率的な薬を開発するための革命的なアプローチとして登場しました。 最近の開発によると、英国のNHSは、UDCAに反応しない患者のための2025年に、デアフィブラノール(Iqirvo®)を承認し、第一次胆管支炎治療市場調査における重要なマイルストーンをマークし、革新的な第二線治療へのアクセスを拡大しました。
- ノベル医薬品の普及:第一次胆道角炎は第一線療法として尿道酸(UDCA)で伝統的に扱われました。 しかしながら、UDCAに十分に反応しない患者の40%近くで、代替治療オプションにはかなりのアンメットが必要でした。 PBCに関与する特定の病気の経路を標的する新しい精密療法を開発することに焦点を合わせるこの薬剤の製造業者を促しました。 最後の5年だけでは、米国FDAや欧州医学機関(EMA)などの規制機関(Ocaliva)、ベザフィブレート(Pemptor)、ミリキズマブ(Kineret)などのフィブリック酸誘導体(Pemptor)、およびミリキズマブ(Kineret)などのインターロイキン12/23阻害剤によって承認されています。 従来の治療と比較して、これらの新規医薬品は、臨床試験における生化学的反応および不完全な生化学的反応のより高い率を実証しています。
第一次性胆嚢炎の治療市場機会
- 組み合わせの採用の増加 療法:コンビネーション療法は、世界的な第一次胆道角膜炎治療市場での成長を促進するために重要な潜在能力を有します。 医療専門家によって、2つ以上の治療オプションの組み合わせは、プライマリ胆管支炎(PBC)に苦しむ患者のためのより良い臨床的反応を達成するのに役立ちます。 PBCは、時間の経過とともに肝臓内の小さな胆管を遅くする自己免疫疾患です。 ursodeoxycholic酸(UDCA)およびobeticholic酸のような現在の処置の選択は、すべての患者が単一の薬剤の療法に等しく反応するある程度に軽減を提供します。 世界保健機関(WHO)からの医療報告は、最大であることを示唆 50~ 60% の患者は UDCA に応答し、不十分な応答と残ります。 これは、組み合わせ療法が違いを生むことができる場所です。 他の免疫調節薬とUDCAを組み合わせることは約束を保持します。 最近の臨床研究では、UDCAとフィブリック酸誘導体を組み合わせることが示されています。例えば、ベザフィブレートは、UDCAの部分的反応器や非応答体内の生化学的、および組織的反応を改善しました。 同様に、UDCAとモノクローナル抗体を組み合わせて特定の炎症経路を標的させることにより、モノサーパイに対する治療効果が向上しました。 対向フェーズ 3 臨床試験は、他のエージェントと合成葉酸の結合や結合などの免疫調節剤と組み合わせてUDCAの安全性と有効性を評価します。 そのような組み合わせ療法試験からの肯定的な結果は、PBCのより良い管理で長い道のりに行き、忍耐強い結果を改善することができます。 これは、PBC治療のための医師やヘルスケアプロバイダーの間で、組み合わせ薬の養生薬の採用の増加が増加する可能性があります。 組み合わせのアプローチの利点に関する臨床的証拠を成長させることは、既存の患者プールを超えてより高い治療のアップテークを駆動することが期待されます。これにより、予測期間にわたって新しい治療の開発と精密ケアモデルに焦点を当てて、主要な胆道治療市場予測を加速します。
第一次性胆嚢炎治療市場動向
- 企業間の戦略的アライアンスとコラボレーション:企業間の戦略的アライアンスとコラボレーションは、近年、世界的な第一次胆道性角膜炎治療市場でますます一般的になっています。 力を合わせて、企業は、研究の専門知識、臨床試験ネットワーク、製造能力、マーケティングなどの補完的な強みを一緒にプールし、医薬品開発を加速し、より優れた患者にサービスを提供しています。 たとえば、臨床段階のバイオ医薬品会社であるCymaBay Therapeutics, Inc.は、2023年1月8日、製薬会社であるKakaken Pharmaceutical Co., Ltd.と共同でライセンス契約を締結し、CymaBayの調査薬の日本における開発および商品化のために、第一次胆管支炎の治療のためのseladelparに入ったと発表しました。 このような戦略的アライアンスの増加により、企業は、グローバル規模での一次胆性角膜炎などの希少疾患に対する効果的な研究、開発、および商品化の課題に対処することが不可欠であることを認識しています。 新規治療の可用性を加速することにより、最終的に患者に利益をもたらします。
最近の開発
- 6月2025日 GSKについて 米国食品医薬品局(FDA)は、ラインリキシバット、経口胆汁酸トランスポーター(IBAT)阻害剤のニュードラッグアプリケーション(NDA)を承認し、第一次胆道胆管支炎(PBC)を有する患者における胆嚢胞を治療することを発表しました。
- 2025年5月、ミルム医薬品は、新28週間の発見を発表しました。 フェーズ2b VANTAGEは、肝臓(EASL)の研究のための欧州連合会で、その経口IBAT阻害剤の揮発性症が第一次胆嚢炎(PBC)の患者で大幅に改善された症状を示す。
- バイオ医薬品グループであるIpsenファーマ(Ipsenファーマ)と、バイオ医薬品グループであるGENFIT(GeneFIT)は、ピボタルELATIVE Phase III試験の正式なトップラインデータを発表しました。 試験では、精巧な肝疾患、第一次胆道角炎(PBC)の患者の治療のために評価され、治療療法、尿道酸(UDCA)の現在の標準に不十分な応答または不耐性を持っている、精巧な肝疾患の患者の治療のために評価されています。
アナリストオピニオン(エキスパートオピニオン)
第一次Biliary Cholangitis (PBC)の処置の市場の価値は2つの第一次力によって運転される長期間にわたる変形を経ます:ursodeoxycholicの酸(UDCA)のmonotherapyおよび原子力受容器の変調器の新進んだクラスとの高められた臨床dissatisfaction上昇–most notably、farnesoid Xの受容器(FXR)のアゴニストおよびperoxisomeのproliferator活動化した受容器(PPAR)のアゴニスト。
UDCAが第一線治療を続けながら、 30%~ 40%の患者は、生化学的反応、英国PBC研究(2016)などの大きなコホーツで一貫して報告され、実際の規制で検証されなかった。 生化学的非応答集団は、臨床的に明確かつ商業的にアドレス指定可能なセグメントを表しています。これは、インターセプト医薬品やジェンフィットなどの現在のプレイヤーが適切に標的しています。 しかし、ほとんどのメーカーは、特に第二線空間で加速規制の牽引を与えられた、緊急この市場の要求に作用することができません。
PBCの唯一の承認されたFXRアゴニストであるObeticholicの酸(OCA)は、相IIIのPOISE試験のアルカリリンカターゼ(ALP)およびGGTレベルの統計的に重要な減少を示しました。 しかし、その商業的な成功は、長期的解決策としてそれを採用するために、ハリス関連の公差の問題と肝専門医の間で再発する2つの要因によってますますます禁忌です。 これは、二重作用分子の明確な開口部を作成します。 Elafibranorは、例えば、デュアルPPAR-α/δアゴニストであるELATIVE Phase IIIの試験から有望なインシムデータを実証し、通常はFXRアゴニストと見なさずに患者の約47%でALP正規化を示す。
さらに、米国および欧州の規制枠組みは、バイオケミカル非応答体に取り組むセカンド・ライン・エージェントが加速する経路を支持し始めています。これは、Orphanの薬物設計と新規参入者のための高速トラック承認によって実証されています。 これらの規制上のインセンティブ, 高いアンメットの必要性と明確なバイオマーカーエンドポイントと結合, PBC は、バイオテクノロジー投資のためのユニークな魅力的なセグメントを作る.
私の評価では、市場は、胆汁酸代謝、線維ジェネシス、免疫調節を同時調整するコンビネーションレジメンへのモノパスウェイターゲティングからピボットに表彰されます。 特に差別化された安全プロファイルを持つ二重または三重作用分子に早期に投資するStakeholderは、市場シェアだけでなく、処方の好みをコマンドします。
市場区分
- 処置のタイプによって
- ウルソデオキシコリン酸(UDCA)
- 酢酸(オカリバ)
- その他(火薬(Tricor)等)
- 流通チャネル
- 病院薬局
- 小売薬局
- オンライン薬局
- 地域別
- 北アメリカ
- アメリカ
- カナダ
- ラテンアメリカ
- ブラジル
- アルゼンチン
- メキシコ
- ラテンアメリカの残り
- ヨーロッパ
- ドイツ
- アメリカ
- スペイン
- フランス
- イタリア
- ロシア
- ヨーロッパの残り
- アジアパシフィック
- 中国・中国
- インド
- ジャパンジャパン
- オーストラリア
- 韓国
- アセアン
- アジアパシフィック
- 中東
- GCCについて 国土交通
- イスラエル
- 中東の残り
- アフリカ
- 南アフリカ
- 北アフリカ
- 中央アフリカ
- 北アメリカ
- 主な胆管支炎治療市場におけるトップ企業
- インターセプト製薬株式会社
- ハイライト治療薬、S.L.
- GSK plc。
- ブリストル・マイアーズ・スクイブ&カンパニー
- エナンタ医薬品
- NWバイオ医薬品
- メルク&株式会社
- Ipsenファーマ
- ジョンソン&ジョンソン
- ジェネフィット
- アイアンウッド医薬品株式会社
- ノバルティスAG
- コース 医薬品
- 株式会社カケン製薬
ソース
第一次研究 次のステークホルダーからのインタビュー
ステークホルダー
- 肝専門医、消化器専門医、移植専門医、病院薬局ヘッド、臨床試験コーディネーター、および患者の擁護団体が北米、欧州、アジア太平洋を横断するインタビュー
データベース
- 世界保健機関(WHO)グローバルヘルス展望台
- Orphanet希少疾患データベース
- 米国国立医学図書館 – 臨床トライアル.gov
- 欧州医薬品庁(EMA) データポータル
- FDAのOrphanの薬剤プロダクト指定データベース
- グローバルヘルスデータ交換(GHDx)
- インド保健福祉省 保健福祉統計
- 中国保健統計年表
- 厚生労働省 希少疾患報告
雑誌
- ファーマタイムズ
- 医薬品技術
- 遺伝子 – 遺伝子工学・バイオテクノロジー ニュース
- 医療ニュース今日 – オートミューン & 肝臓セクション
- 創薬・開発
- Fierce Biotech - 肝臓とAutoimmuneの更新
- ファーマフォーカスアジア
- MedTechの展望
ジャーナル
- ヘパトロジージャーナル
- ヘパトロジー(AASLD)
- 臨床消化器科学と肝疾患
- 自動免疫学会
- 医薬品・医薬品
- 希少疾患のオルファネットジャーナル
- 薬物安全
- ランセット・ガストロエンテロジー&ヘパトロジー
新聞
- ニューヨークタイムズ – 健康セクション
- 金融タイムズ – グローバル医薬品
- ガーディアン – ヘルスケアイノベーション
- ビジネススタンダード - インドバイオテクノロジー&ファーマ
- Handelsblatt – ヨーロッパの医薬品市場カバレッジ
- 日本タイムズ – 健康・医薬品開発
協会について
- 肝疾患研究協会(AASLD)
- 肝臓の研究のための欧州連合(EASL)
- アジアパシフィック協会(APASL)
- 国際Autoimmune Hepatitisグループ
- 肝臓の研究のためのインド国立協会 (INASL)
- 患者組織の国際連合(IAPO)
- カナダのライバー財団
- 世界の肝炎 パートナー
パブリックドメインソース
- 米国国立衛生研究所(NIH)
- 欧州委員会公衆衛生報告書
- インドの医薬品部門
- 厚生労働省(日本)
- 中国国家医療製品管理(NMPA)
- OECD健康統計
- 世界銀行 – ヘルスケアアクセスと病気バーデンレポート
- 保健福祉省(英国)
独自の要素
- ログイン 過去8年間、データ分析ツールとCMIの既存の情報リポジトリ
*定義:第一次胆道角炎は、肝臓の小さな胆管が炎症を起こし、最終的に破壊される慢性疾患です。 胆管がない場合、胆汁が蓄積し、肝臓の損傷を引き起こします。 時間が経つにつれて、この損傷は肝臓の瘢痕、肝硬変、そして最終的に肝障害につながることができます。
著者について
Ghanshyam Shrivastava - 経営コンサルティングとリサーチの分野で 20 年以上の経験を持つ Ghanshyam Shrivastava は、プリンシパル コンサルタントとして、生物製剤とバイオシミラーに関する幅広い専門知識を持っています。彼の主な専門知識は、市場参入と拡大戦略、競合情報、さまざまな治療カテゴリと API に使用されるさまざまな医薬品の多様なポートフォリオにわたる戦略的変革などの分野にあります。彼は、クライアントが直面する主要な課題を特定し、戦略的意思決定能力を強化するための堅牢なソリューションを提供することに優れています。彼の市場に関する包括的な理解は、リサーチ レポートとビジネス上の意思決定に貴重な貢献をします。
Ghanshyam は、業界カンファレンスで人気の高い講演者であり、製薬業界に関するさまざまな出版物に寄稿しています。
独占トレンドレポートで戦略を変革:
よくある質問