リアルワールドデータ(RWD)市場分析と予測:2025-2032
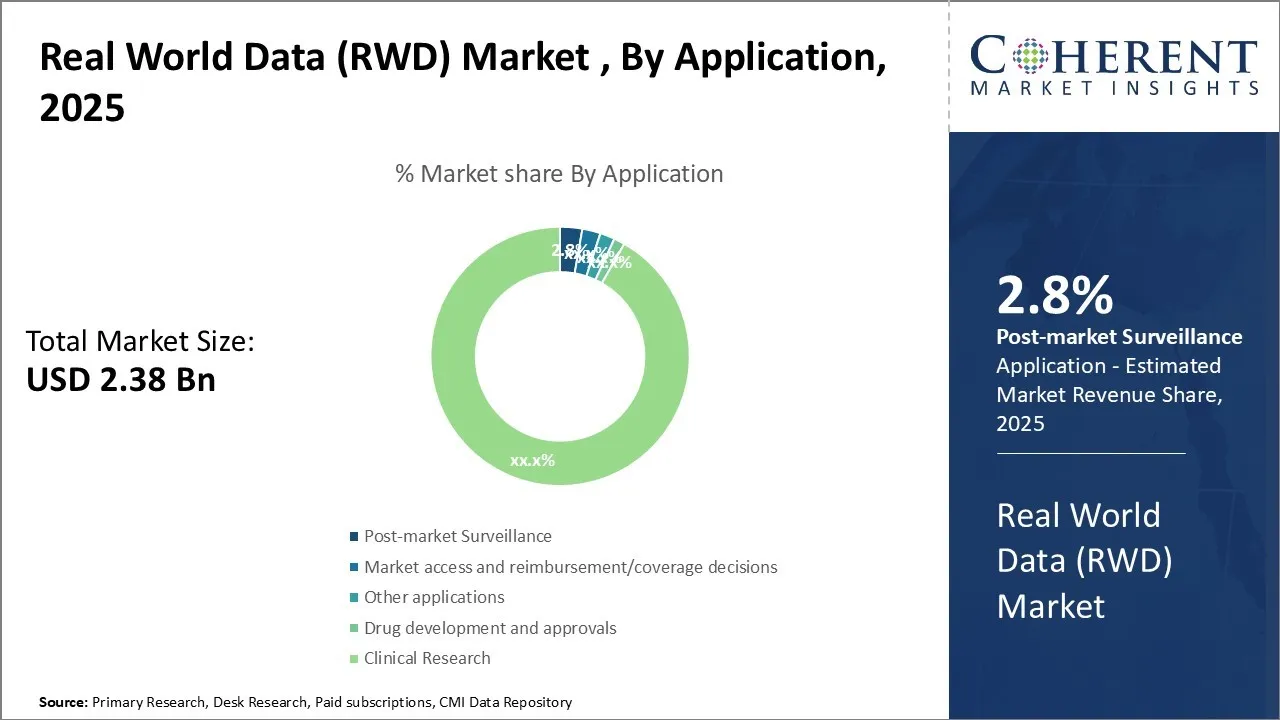
リアルワールドデータ(RWD)市場規模は、 米ドル 2.38 Bn 2025年、到達見込み 米ドル 6.1 Bn 2032年、化合物の年間成長率(CAGR)を展示14.4%2025年~2032年
キーテイクアウト
- アプリケーションにより、市場監視セグメントは、2025年までに約30%の現実世界データ市場の最大のシェアを保有し、継続的な安全監視と市販薬や医療機器の有効性評価の必要性によって駆動されます。
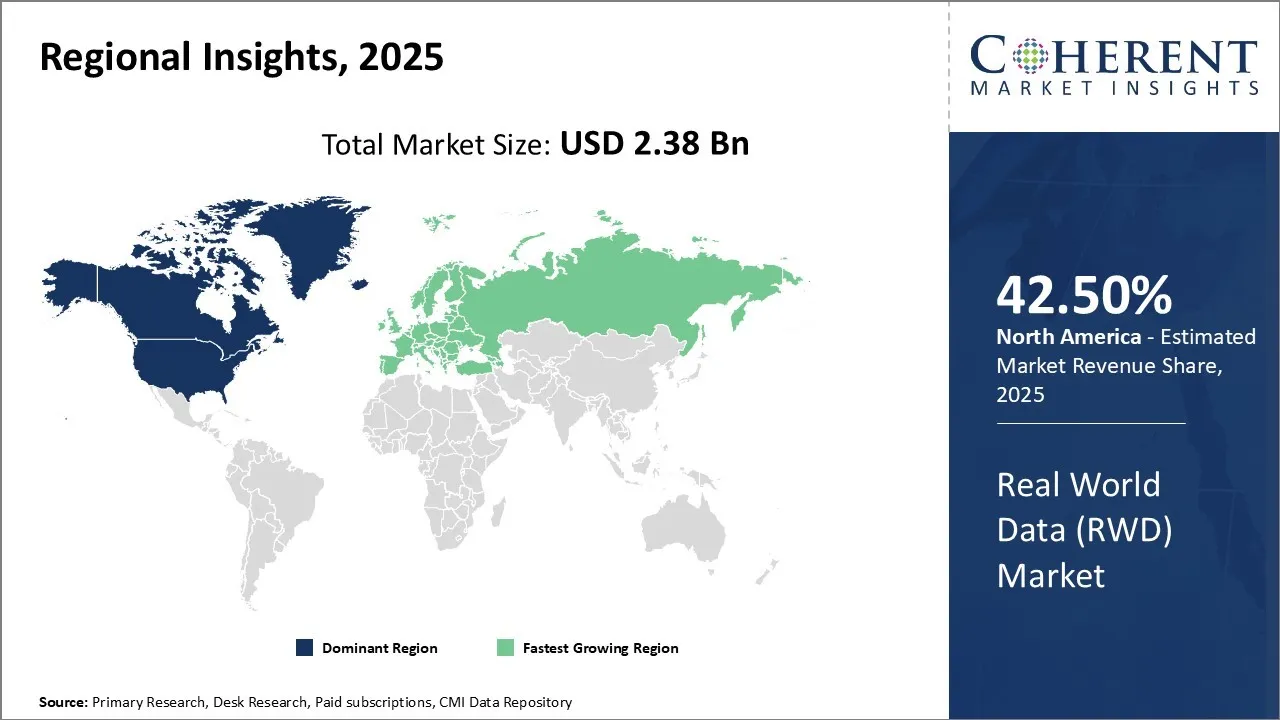
- 地域別では、北米は、2025年にグローバル・リアル・ワールド・データ・マーケット・アウトルックを率いて、42.5%の市場シェアを推定し、先進医療インフラ、電子健康記録(EHR)の普及、現実世界証拠(RWE)の使用を促進する強力な規制枠組みを拡充しました。
- 欧州は、第2位の市場として位置付けられ、2025年に約28.5%の市場シェアを保持すると予想され、デジタルヘルス技術への投資を増加させ、医療関係者間のコラボレーションを増加させました。
- アジアパシフィック地域は、2025年までに予想される強固な化合物の年間成長率(CAGR)で急速に成長する市場として生まれ、ヘルスケアの普及、デジタルインフラの拡大、RWDの採用を奨励する政府の取り組みによって推進されています。
市場概観
RWDの採用増加医薬品開発そして承認、市場アクセス、および市場監視は市場の成長を運転しています。 RWDは実際の設定から収集したデータです。電子健康記録(EHRs)、クレームデータ、患者登録 医薬品や医療機器の安全性と有効性に関するエビデンスを生成し、患者様の結果に対する治療の影響を評価することができます。
現在のイベントと現実世界データ(RWD)市場への影響
イベント | 記述および影響 |
RWDの統合に影響を与える規制開発 |
|
データインフラにおける技術開発 |
|
ジオポリティカル データガバナンス チャレンジ |
|
75 以上のパラメータに基づいて検証されたマクロとミクロを発見: レポートにすぐにアクセス
パイプライン分析
リアルワールドデータ(RWD)市場成長は、複数の臨床開発段階にわたって医薬品候補の堅牢なパイプラインによってサポートされています。 これらの候補者は、多様な患者集団における安全性、有効性、および治療結果への洞察を高める、承認および商品化により、実質的な世界的証拠を生成することが期待されます。
フェーズIII 候補者:
- Tezepelumabの特長 — イノベーターとスポンサー:アムゲンとアストラゼネカ
- Efgartigimodの特長 — イノベーターとスポンサー:Argenx
フェーズII 候補者:
- Deucravacitinib(ドゥクラバシチニブ) — イノベーター&スポンサー: ブリストル・マイアーズ・スクイブ
- Zuranoloneの — イノベーターとスポンサー:セージ治療薬とバイオジェン
- マキシシニブ —イノベーター&スポンサー:ABサイエンス
フェーズIの候補者:
- アレオ-715 — イノベーターとスポンサー:アローネ治療薬
- NBIb-1817 (キセノン1817) — イノベーター:キセノン製薬、スポンサー:ネロクリンバイオサイエンス
- OP-1250の特長 — イノベーターとスポンサー: Olema Pharmaceuticals
プレクライニングの候補者:
- BDTX-1535の特長 — イノベーター&スポンサー:ブラックダイヤモンド治療薬
- DSP-0038の特長 — イノベーター&スポンサー:住友ダイニポン 薬局
- NX-1607の特長 — イノベーター&スポンサー:Nkarta Therapeutics
これらのパイプライン分子は、さまざまな治療分野に及ぶ、RWDを活用して、スポンサーやイノベーターの成長の関心を反映し、規制当局の承認、市販後の監視、およびパーソナライズされた医療戦略をサポートします。
特許文献
RWD市場予測は、業界リーダーや新規市場参入者からの投資によって燃料供給される特許の急速に進化し、拡大するエコシステムを経験し、分析、統合、およびアプリケーション技術の競争優位性を獲得しています。 RWDに関する特許は、主にデータ収集システム、データ匿名化、AIベースの分析、相互運用性の問題のインフラの進歩に懸念しています。
さらに、世界最大の製薬会社、ITビジネス会社、ヘルスケア分析会社が、新たなアルゴリズムやプラットフォームを積極的に特許化し、現実の証拠生成を自動化し、データを充実させ、規制要件の遵守を確保しています。 最近の特許は、ブロックチェーンやその他のデータ共有の安全な方法の使用に焦点を当て、機密性の高い健康情報に関連するプライバシーとセキュリティリスクを削除し、全体的なプライバシーと健康データのセキュリティを強化します。
この特許活動の地理的濃度は、特許および高品質の知的財産システムのための事前および明確に定義された規制枠組みがある、北アメリアとヨーロッパにあります。 しかし、アジア太平洋地域の新たな特許出願は、この地域のRWD技術において、いくつかの増加した関心と革新的な活動を提案しています。
一般に、進化する特許の地理と新興特許の焦点は、RWD市場とフロンティアの競争の増加を示し、技術開発と市場差別に関する知的財産の高まりの重要性を強調しています。
払い戻しシナリオ
リアル・ワールド・データ(RWD)の償還ダイナミクスは、世界中のコーディングスキーム、ガイドライン、保険モデルによって影響を受けています。 RWD の ICD-10、CPT、HCPCS などの重要なコーディングフレームワークは、RWD の補助サービスや、欧州のGDPR のようなデータのプライバシーに関する法律、米国における HIPAA などの適切な分類を提供します。
FDA(米国)、EMA(欧州)、PMDA(日本)は、規制当局として、RWDを利用して、医薬品やデバイス承認に関する決定と、両目的の払い戻しを行う主要な選手です。 HTAボディは、RWDがカバレッジポリシーを通知するために適用される介入の臨床的および経済的価値を評価します。
支出に関して, RWDは、グローバルヘルスケアの支出の分の1分のアカウントだけを関連した支出: 米国で1〜2%, NHSの約0.5〜1% £129.7億予算, 日本とオーストラリアの同様の部分と一緒に. 中国の基本的な医療保険システムは、RWD関連のサービスの合計予算の約0.3-0.5%を費やすと推定されます。
RWDの直接コストが低い一方で、規制当局の承認と価値に基づくケアでRWDの使用が増えることにより、その重要性が高まっています。 本方針は、ヘルスケアシステムにおけるRWDの価値におけるパラダイムシフトを発症する。
リアルワールドデータ(RWD)の規定
リアルワールドデータ(RWD)サプリメントは、患者の状態の変化として、ヘルスケアプロバイダーや開業医にとってピボタルです。 治療の特定の行や疾患段階に応じてRWDシフトに対する臨床医の依存性。 第一線の処置は臨床試験に強く付着し、ガイドラインを定める間、試験設定の反対に薬物の仕事そして安全についての洞察の必要性そして重要による第2ラインおよび後で処置に来るときより多くのRWDの信頼性があります。
疾患の進行は、使用されるRWDスペクトルも変化します。初期病態管理は、臨床試験から来ているエビデンスに従う傾向がありますが、より高度または複雑な段階はRWDに必要のある治療法を微調整するために大きく依存します。 例えば、処方薬は、優勢な試験が有効性をサポートしている確立された薬を使用する傾向がありますが、さらにタイムラインを下げると、彼らのスタンスを変更し、RWDが代替療法または組み合わせ療法を介してより良いパフォーマンスを発揮する他のオプションを見ることがあります。
RWDを優先する他の理由は、患者特性(年齢グループ、既存の病気、民族性)、練習の種類(学術的またはコミュニティ慣行)、医療システム(値ベースまたは有料サービスモデル)によるインセンティブを提供し、電子健康記録やその他の決定支援ツールの形でRWDの使用を含みます。
これらのシナリオでは全体的に, 証拠に限界がある, 処方者は、治療計画によりパーソナライズされたアプローチを作成することになるとき、その多くを組み込むRWDに依存することが示されている.
グローバル・リアル・ワールド・データ(RWD)市場動向
適用の面では、市場監視の部門は最も大きい実質の世界のデータ(RWD)の市場を握るために写っています 2025年までに約30%のシェアは、主にリリース後の製品の継続的な安全と性能監視に重点を置いた規制を強化することによって駆動されます。 規制当局は、継続的なコンプライアンスを確保し、リスクを軽減するための市場要件を強化するために、市場要件を強化します。組織は、包括的な監視戦略を優先しています。
市場監視システムは、メーカーや規制機関が、製品性能や有害事象に関連する現実的なデータを体系的に収集、分析し、行動することを可能にします。 これらのシステムは、安全上の懸念をタイムリーに識別することにより、透明性を高め、エンドユーザーを保護し、積極的なリスク管理をサポートします。
さらに、高度なデータ分析とリアルタイムレポートツールの統合により、意思決定プロセスを強化し、迅速な是正措置と規制遵守を保証します。 その結果、患者の安全と規制の過視に対する成長の焦点は、業界全体のポスト市場監視ソリューションの採用を継続しています。
地域洞察
このレポートについてもっと知りたい方は, 無料サンプルをダウンロード
北アメリカの実質の世界のデータ(RWD)の市場分析および傾向
北米は、約42.5%の市場シェアを保持し、2025年に世界規模のデータ市場需要をリードすることを予測しています。 このリーダーシップは、地域の高度な医療インフラ、十分に確立された医薬品およびバイオテクノロジー分野、および医薬品の承認と臨床研究に関する厳格な規制枠組みによって駆動されます。
米国とカナダは、がん、糖尿病、心血管疾患などの慢性疾患の蔓延を増加させ、患者の症状を改善するための包括的な現実世界的証拠を要求することによって支持され、市場成長への主要な貢献です。
洗練された健康ITシステム、広範な電子健康記録(EHR)の採用、および医療意思決定への現実世界のデータの統合を促進する強力な政府の取り組みからの地域の利点。 また、データプライバシーとセキュリティフレームワークへの投資により、大規模な健康データセットの倫理的かつ確実な利用を容易にし、RWD市場拡大を加速します。
ヨーロッパリアルワールドデータ(RWD)市場分析とトレンド
ヨーロッパは2025年に第2位の実世界データ市場価値として、予想される28.5%のシェアとして置かれます。 領域の進歩は、医療イノベーションに重点を置き、臨床研究と政策策定におけるビッグデータ分析の広範な採用に焦点を合わせています。 ドイツ、イギリス、フランス、ノルディック諸国などの国々は、RWDを活用し、ヘルスケア・デリバリー、規制評価、およびファーマコヴィジランを強化する取り組みです。
公衆衛生機関、研究機関、民間部門の選手との強力なコラボレーションにより、RWD活用のための包括的な環境が生まれます。 また、欧州の先進的な規制風景は、一般データ保護規則(GDPR)のような枠組みを含んでおり、患者のプライバシーに対するデータアクセシビリティのバランスをとり、現実世界の証拠生成における信頼と透明性を可能にします。
アジアパシフィックリアルワールドデータ(RWD)市場分析とトレンド
アジア・パシフィックは、グローバル・リアル・ワールド・データ市場において最も急速に成長する地域として、2025年までに予想される10.5%の堅牢なCAGRが誕生しました。 この急激な拡張は、地域の大規模で多様な人口基盤に燃料を供給し、慢性疾患や生活習慣病の負担を増加させ、医療インフラを拡大しています。 中国、インド、日本、東南アジアなどの主要市場は、臨床研究と医療政策におけるRWDの統合に向けた成長政府支援と戦略的取り組みを目撃しています。
デジタルヘルスの採用の増加、健康データのデジタル化の改善、および実質の世界のエビデンス機能に投資するローカルおよび多国籍製薬企業の成長している存在は市場成長を加速します。 また、治療効果を改善し、ヘルスケアコストを削減するRWDのメリットに対する意識を高めることで、公共および民間の医療分野における採用を促進します。
マーケットレポートスコープ
ヨーロッパリアルワールドデータ(RWD)市場レポートカバレッジ
| レポートカバレッジ | ニュース | ||
|---|---|---|---|
| 基礎年: | 2024年(2024年) | 2025年の市場規模: | 米ドル 2.38 Bn |
| 履歴データ: | 2020年~2024年 | 予測期間: | 2025 へ 2032 |
| 予測期間 2025〜2032 CAGR: | 14.4% | 2032年 価値の投射: | 米ドル 6.1 Bn |
| 覆われる幾何学: |
| ||
| カバーされる区分: |
| ||
| 対象会社: | IQVIA Holdings Inc.、Optum、Inc.、Cerner Corporation、Flatiron Health、Inc.、IBM Corporation、Tempus Labs Inc.、Syneos Health Inc.、Evidera、Inc.、Palantir Technologies Inc.、SASインスティテュート | ||
| 成長の運転者: |
| ||
| 拘束と挑戦: |
| ||
75 以上のパラメータに基づいて検証されたマクロとミクロを発見: レポートにすぐにアクセス
グローバルリアルワールドデータ(RWD)市場ドライバー
- 電子健康記録の採用の増加(EHRs):
ヘルスケアプロバイダーによる電子健康記録の普及は、膨大な量の患者データの蓄積につながっています。 このデータは、集約され、匿名化されると、現実世界の患者結果、治療パターン、および病気の進行に貴重な洞察を提供できます。
たとえば、2023年1月16日、富士通、情報通信技術機器・サービス会社、札幌医科大学では、電子健康記録(EHR)(2)、個人健康記録(PHR)など、患者の医療データに対するデータポータビリティを実現する共同事業の立ち上げを発表しました。
- 証拠ベースの医薬品の需要拡大: : :
RWDに由来する実世界証拠(RWE)に依存するエビデンスベースの医薬品に重点を置いています。 規制当局、受給者、および医療従事者を含むヘルスケアのステークホルダーは、治療の有効性、比較効果、安全性、費用対効果に関する情報に基づいた決定を行うために、実際のデータの使用の重要性を認識しています。
たとえば、自然医学雑誌に掲載された記事によると、2023年1月16日、ウェアラブル技術、データサイエンス、機械学習の進歩は、エビデンスを次世代の「ディープ」薬の未来に変えるようになりました。 また、医薬品開発の全てのフェーズをクリニックに成功させるとともに、5~2.5億ドル以上かかります。 そのため、新しい進歩を促進するために、患者を関与し、必要な証拠を生成するために必要な革新的な戦略が必要です。
- 規制対応と指導: : :
米国食品医薬品局(FDA)および欧州医薬品局(EMA)などの規制機関は、規制決定における現実世界証拠の価値を認識しています。 これらは、RWDおよび現実世界の証拠(RWE)の使用のためのガイドラインとフレームワークを規制の提出、薬物承認、および市場監視、さらに現実世界のデータに対する要求を運転しました。
- データ分析と技術の開発: : :
人工知能(AI)、機械学習(ML)、ビッグデータ分析などのデータ分析ツールやテクノロジーの進歩により、大規模で複雑な現実的なデータセットから有意義な洞察の抽出を容易にしました。 これらの技術は、治療パターン、患者サブグループ、有害イベント、およびその他の臨床関連情報を特定するためにRWDの分析を可能にします。
グローバルリアルワールドデータ(RWD)市場チャンス
- 医薬品開発・臨床試験: : :
実際のデータは、医薬品開発プロセスを最適化し、臨床試験設計を強化するために活用することができます。 RWDは、ターゲット人口を識別し、病気の進行状況を理解し、治療の有効性を評価し、潜在的な安全上の懸念を識別するために使用することができます。 実際の証拠を臨床試験に統合することにより、研究者は試験効率を高め、適切な患者をリクルートし、堅牢な結果を生み出すことができます。
例えば、2022年6月、医薬品会社であるAbbVie Inc.は、AbbVie Research Collaborativeの発足を発表しました。米国の成人がAbbVieの世界的な科学研究者と提携できるようにする健康データプラットフォームです。 共同参加者は、遺伝子、生活習慣、運動情報、医療記録などの現実的な健康データに貢献し、より包括的な健康写真を提供します。 実際の健康データは、研究者が臨床試験内で見られない健康や病気のパターンを見つけることを可能にします。
- 比較効果研究: : :
実際のデータでは、現実世界の設定におけるさまざまな治療オプションの利点とリスクを比較することに焦点を当てた比較の有効性の研究を可能にします。 RWDは、多様な患者集団における治療の有効性、安全性、および患者様による結果の評価を可能にし、医療の意思決定のための貴重な洞察を提供します。
たとえば、2020年8月には、医療機器イノベーションコンソーシアム(MDIC)は、ウイルス診断における規制決定のための現実世界証拠(RWE)フレームワークの発売を発表しました。
グローバルリアルワールドデータ(RWD)市場動向
- データソースの統合の増加: : :
患者の健康と結果の包括的なビューを得るために、複数のデータソースを統合する成長傾向があります。 これは、電子健康記録(EHR)、クレームデータ、患者登録、ウェアラブルデバイス、ソーシャルメディアデータ、およびゲノム情報を組み合わせたものです。 多様なデータソースを統合することで、より包括的な分析を可能にし、より豊かな洞察を現実的な患者体験と成果に提供します。
- データ分析とAIの高度化: : :
人工知能(AI)や機械学習(ML)など、データ分析ツールや技術における世界的なリアルタイムデータ(RWD)市場は急速に進んでいます。 これらの技術は、従来の統計的なアプローチでは明らかではないかもしれないパターン、傾向、および相関を明らかにする、大きくて複雑なデータセットのより洗練された分析を可能にします。 AI と ML アルゴリズムは、データ統合、予測モデリング、リスクのストラティフィケーション、意思決定のサポートを支援できます。
たとえば、2021年8月、医薬品会社であるSyneos Healthは、ヘルスケア技術会社であるAetionと提携し、実際の証拠ソリューションを提供し、分析主導のデータと規制レベルのデータを提供します。
アナリスト視点
- リアルワールドデータ(RWD)市場は、ヘルスケアにおけるエビデンスベースの意思決定の需要増加と、電子健康記録(EHR)の展開の増加による増加の需要増加による強力な成長軌道上にあります。
- RWDは、創薬、臨床試験、およびポストマーケティングの監視に集中しています。ステークホルダーは、患者の成果と現実的な治療効果を理解することを目指しています。
- パーソナライズされた医療の必要性と慢性疾患の管理は、ヘルスケアシステム全体でRWDの採用を大幅に加速しています。
- 主要な成長阻害剤は、データプライバシーとセキュリティ、データフォーマットの標準化の欠如、プラットフォーム全体の限られた相互運用性に対する永続的な懸念を含みます。
- 高いインフラコストと技術的な障壁は、限られたデジタル成熟度を持つ小規模なヘルスケアプロバイダーとシステムの間で採用が遅くなる可能性があります。
- これらの課題にもかかわらず、市場は技術革新の可能性を秘めています。特にAIと機械学習の統合を通じて、データ分析、パターン認識、予測的な洞察を変革しています。
- 製薬会社、ヘルスケアプロバイダー、およびペイアー間のコラボレーションは、高度な分析および可視化プラットフォームの開発を推進し、生態系を強化しています。
- 北米は、堅牢な医療インフラ、高デジタルペネトレーション、規制対応により、グローバルRWDランドスケープを継続的に推進しています。
- アジア・パシフィックは、医療投資、政府支援のデジタル健康への取り組み、インドや中国などの人口の多い国で病気の負担が増加するなど、急速に成長する地域として誕生しています。
リアルワールドデータ(RWD)市場:主要開発
- 2025年4月15日 IQVIAの特長 AIと自然言語処理(NLP)を活用した次世代RWD分析プラットフォームを立ち上げ、ライフサイエンス企業向けの実世界証拠生成の加速を目指します。 プラットフォームは、複数のソースのデータセットを横断し、より高速なインサイトを提供します。
- 2025年3月25日 フラットアイアンヘルス 米国における主要な腫瘍学ネットワークとの戦略的パートナーシップを締結し、実際の腫瘍学データエコシステムを拡充 EHR-derivedの臨床データを幅広く統合し、がん治療分析と医薬品開発を強化します。
- 2025年2月6日、Optumは、データ透明性、トレーサビリティ、患者様の同意管理を改善するために設計されたブロックチェーンベースのRWD共有プラットフォームを導入しました。 大規模な医療データ連携の確保に向けた重要な取り組みです。
- 2025年1月、HealthVerityは、100を超えるソースから非識別、リンクされたデータ資産を提供するクラウドネイティブRWD市場を発表しました。 プラットフォームは、医薬品、ペイア、およびプロバイダの利害関係者のための現実的なデータセットへのアクセスを簡素化することを目指しています。
市場区分:
- コンポーネント:
- サービス
- データセット
- 臨床設定 データデータ
- クレームと請求データ
- ファーマシーデータ
- レジストリベースのデータ
- 患者主導のデータ
- 適用によって:
- 医薬品開発・承認
- 市場アクセスと払い戻し/カバー決定
- 市場調査
- 臨床研究
- その他のアプリケーション
- エンドユーザー:
- 医薬品・医療機器会社
- 医療従事者
- ヘルスケアプロバイダー
- 政府機関
- その他
- 地域別:
- 北アメリカ
- ヨーロッパ
- アジアパシフィック
- ラテンアメリカ
- 中東
- アフリカ
- グローバル・リアル・ワールド・データ(RWD)市場におけるトップ企業
- 株式会社IQVIAホールディングス
- 株式会社オプタム(ユナイテッドヘルスグループ)
- サーナー株式会社
- フラットアイアンヘルス株式会社
- IBMコーポレーション
- テンパスラボ株式会社
- シナオスヘルス株式会社
- Evidera株式会社
- パランサー・テクノロジーズ株式会社
- SASインスティテュート株式会社
ソース:
第一次研究インタビュー
- 主なオピニオンリーダー(KOL)
- 産業専門家
- ヘルスケアプロフェッショナル
- レギュレーションボディ
- その他
データベース
- 国民の健康と栄養検査調査(NHANES)
- FDA有害事象報告制度(FAERS)
- メディケア・メディケイドサービスセンター(CMS)
- 臨床実践研究データリンク(CPRD)
- その他
雑誌
- ヘルスケア情報学
- 医療経済学
- 健康データ管理
- ヘルスケアIT ニュース
- その他
ジャーナル
- アメリカン・メディカル・インフォマティクス協会ジャーナル(JAMIA)
- JMIR医療情報学
- BMC医療情報学と意思決定
- その他
新聞
- ウォールストリートジャーナル
- ニューヨークタイムズ
- 金融タイムズ
- ワシントンポスト
- その他
協会について
- ヘルスケア情報管理システム協会(HIMSS)
- アメリカンメディカルインフォマティクス協会(AMIA)
- 医療機器メーカー協会(MDMA)
- HL7インターナショナル
- その他
パブリックドメインソース
- 世界保健機関(WHO)
- 国立衛生研究所(NIH)
- 疾病対策センター(CDC)
- 欧州医薬品庁(EMA)
- その他
独自の要素
- ログイン データ分析ツール
- プロモーション CMI 過去8年間の情報の登録
*定義:リアルワールドデータ(RWD)とは、患者の健康状態を反映した様々な情報源から収集したデータ、および/または実際の設定におけるヘルスケアの配信を指します。 実際のデータは、電子健康記録(EHR)、クレームおよび請求活動、製品および病気の規制、外来または入院設定における患者関連の活動、健康監視装置、およびその他の情報源などのさまざまな情報源から収集され、従来の臨床試験のデータとは対照的に、管理された条件下で収集されます。 製品の使用に関するこのデータ、実際の証拠(RWE)、および医療分析および意思決定に使用するための利点または欠点が生成されます。
著者について
Komal Dighe は、市場調査とコンサルティングで 8 年以上の経験を持つ経営コンサルタントです。彼女は、ヘルステック コンサルティング レポートで高品質の洞察とソリューションを管理および提供することに優れています。彼女の専門知識は、一次調査と二次調査の両方の実施、クライアントの要件への効果的な対応、市場の推定と予測に優れています。彼女の包括的なアプローチにより、クライアントは徹底的かつ正確な分析を受けられるため、情報に基づいた意思決定を行い、市場の機会を活用できます。
独占トレンドレポートで戦略を変革:
よくある質問