細胞治療の市場規模と予測 – 2025 年から 2032 年
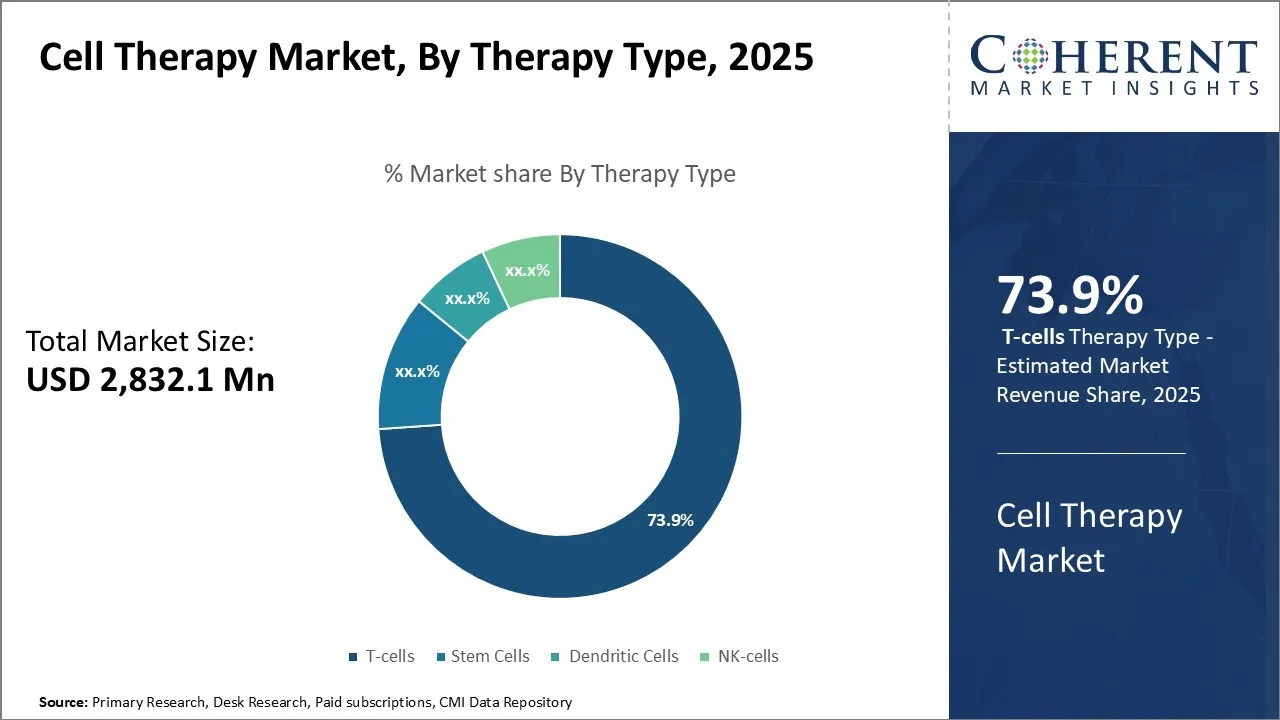
世界の細胞療法市場は、2025 年に28 億 3,210 万米ドルと推定され、2032 年までに53 億 8,340 万米ドルに達すると予想されており、年間複合成長率を示しています(CAGR) 9.6% の2025 年から 2032 年まで。
重要なポイント
- 治療法の種類別では、がんの発生率の上昇により、T 細胞が73.9%という最大の市場シェアを維持します。
- 適応症別では、遺伝子工学と細胞技術の進歩により、オンコロジーは 2025 年に70.2%の最大の市場シェアを保持すると予想されています。
- エンドユーザー別では、先進的なインフラストラクチャと医療サービスのおかげで、病院は 2025 年に 41.7% という卓越した市場シェアを獲得しました。 臨床能力
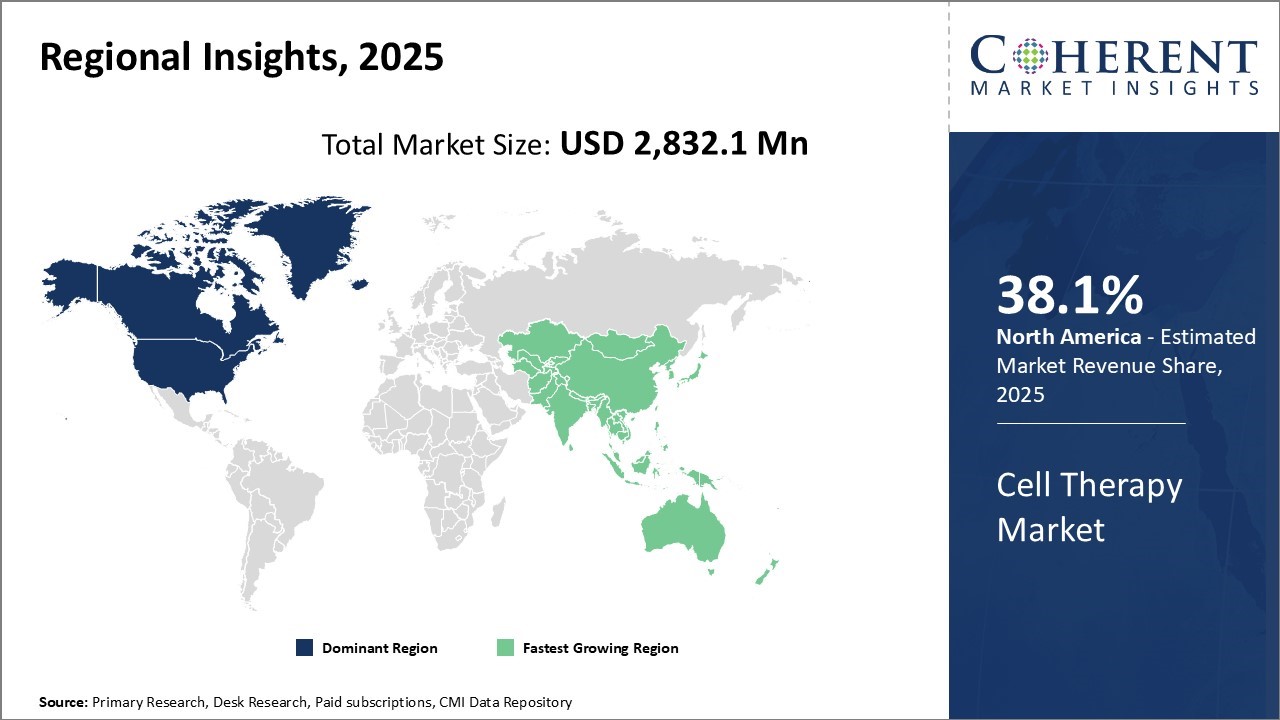
- 地域ごとに見ると、北米は強力な研究開発エコシステムと強力な研究開発エコシステムにより、2025 年には38.1% の推定シェアを獲得し、市場全体を支配しています。 臨床試験インフラストラクチャ
市場概要
世界の細胞療法市場は、再生医療、免疫療法、遺伝子工学の進歩によりイノベーションが促進され、急速に拡大しています。 研究者や企業は、腫瘍学、希少疾患、自己免疫疾患を治療するためのCAR-T 細胞、幹細胞、TCR 療法などの治療法を開発しています。 慢性疾患や遺伝性疾患の症例の増加に加え、支援的な規制の枠組みや強力な臨床パイプラインが需要を押し上げています。 病院や専門治療センターは、これらの治療法を実施するためのインフラストラクチャを構築しており、その一方で、技術革新と戦略的コラボレーションにより、世界中でアクセシビリティと商業化が向上しています。
現在のイベントとその影響 細胞療法の市場
現在のイベント | 説明とその影響 |
主要地域における規制整備 |
|
技術開発とイノベーション |
|
投資・資金調達風景 |
|
75 以上のパラメータに基づいて検証されたマクロとミクロを発見: レポートにすぐにアクセス
細胞療法の市場 洞察力、療法のタイプによって: T-Cellsは、その市場が最も高いシェアに貢献 堅牢な研究開発投資と臨床パイプライン。
Tセルは2025年に73.9%の最大の市場シェアを保持しています。 T細胞またはTリンパ球は、適応免疫システムの重要な部分を形成し、感染または癌細胞を認識することができます。 近年の研究では、従来の薬が除去できない癌細胞を識別し、破壊するために、CAR T細胞療法として知られるT細胞を設計する可能性が示されています。 KymriahやYescartaなどの先駆的な薬は、血液癌の段階的な臨床試験で印象的な完全寛解率を達成しました。 規制機関によるその後の承認は、CAR T-cell療法を主流治療オプションとして検証しました。 T-cellセグメントに電力を供給する主な要因には、T-cellの生物学と免疫学の理解が向上し、T-cellエンジニアリングおよび拡張のための新技術の開発、T-cellの移植を改善するためにリンパ節療法の改良、および新規腫瘍評価抗原の識別が含まれます。 たとえば、インドは2025年11月に、IIT BombayのスピンオフであるImmoACTが開発した、初の無二のCAR-T細胞治療を発売することにより、がん免疫療法へのアクセスを拡大しました。
細胞療法の市場 インディケーションによるインサイト: オンコロジーは、その市場へのオウイングの最高のシェアに貢献します 投資および資金調達の増加。
2025年に最大70.2%の市場シェアを占めるオノロジー。 腫瘍学のセグメントは、血液および固体癌の高有効性として、細胞療法市場を強く促進し、従来の治療の制限は、緊急の要求を作成します。 研究者や企業は、がんケアの精度と有効性を向上させるために、CAR-T、TCR、およびその他の免疫細胞療法を促進しています。 堅牢な臨床パイプライン、成功した試験結果、および支持的な規制措置は、採用を強化しています。 たとえば、2025年5月、HCGマナバタがんセンターとSunAct – アドバンストがん治療は、HCGMCC、Nashik、Shripad Banavali、Paediatric Haemato-Oncologyの議長、Tata Memorial HospitalのIndian Academy of Paediatrics and Academic Director、MumbaiのIndian Academy of PaediatricsとAcademic Directorの4ヵ国センターを開設しました。
細胞療法の市場 エンドユーザーによるインサイト: 病院は、その市場に出ている最高のシェアに貢献します リスク・副作用の管理経験
病院は、2025年に41.7%の著名な市場シェアを獲得しました。 病院は、複雑な治療を提供するために必要なインフラと臨床専門知識を提供することで、細胞療法市場を積極的に推進します。 それらは安全な管理および副作用を管理するためにICUs、注入の中心および専門にされた実験室を作動させます。 病院は臨床試験を実施し、臨床検査をサポートし、患者が革新的な治療に早期アクセスできるようにします。 受給者との強固なつながりと払い戻しプロセスにおける経験は、治療の採用を促進します。 さらに、病院は製造能力に投資し、先端技術を統合し、戦略的パートナーシップを形成し、細胞療法サービスを拡大し、患者のアクセスを高めます。 例えば、2025年10月、レジリエンスとMDアンダーソンがんセンターの合弁であるCTMCは、ブラジル・サンパウロにあるエインスタイン病院イスラエルータと共同で、ブラジルとラテンアメリカの細胞療法の採用を加速しました。
AI(人工知能)の役割 細胞療法の市場
人工知能(AI)は、研究、開発、製造プロセスの高度化により、細胞療法市場を積極的に変革しています。 AIアルゴリズムは、複雑な生物学データを分析し、最適な細胞ターゲットを特定し、治療結果を予測し、薬物発見を加速します。 製造業では、AIは品質管理を高め、細胞の拡張を最適化し、一貫した結果を保障します。 また、治療をパーソナライズし、患者の反応を監視することにより、臨床的意思決定を導きます。 開発を合理化し、精度を高め、エラーを最小限に抑えることにより、AIは企業やヘルスケアプロバイダーがより安全で効果的で、アクセス可能なセルセラピーを実現することができます。 たとえば、2025年2月、セルリーノは、世界初の病院ベースのオートロジスiPSCファウンドリーを起動するために、マスジェネラルブリガムの遺伝子と細胞療法研究所と提携しました。 チェリーノのAI主導のNebla技術を使用して、イニシアチブは、パーソナライズされたセルと組織のセラピーを直接ケアする分散型ハブの全国ネットワークを作成することを目指しています。
地域洞察
このレポートについてもっと知りたい方は, 無料サンプルをダウンロード
北アメリカ 細胞療法の市場 トレンド
北アメリカは2025年に38.1%の推定株式と全体的な市場を支配します。 北米の細胞療法市場は、企業が、先進的な製造インフラと強力なR&D能力を活用し、アポジティブな「オフ・ザ・シェルフ」プラットフォームを開発するにつれて急速に進化しています。 大手バイオテクノロジーハブは、モジュラー、自動生産モデルを拡張し、効率性を高めています。 米国FDAの指定を含む加速された規制経路は、より速い臨床進歩を可能にし、堅牢なペイアproviderネットワークおよび病院ベースの細胞療法センターは患者のアクセスを改善します。 Biopharmaの会社およびCMOsは地域を渡る療法の商品化そしてスケール配達を合理化するために戦略的パートナーシップを形作ります。 たとえば、2025年10月、Visionary Holdings Inc.は、カナダに拠点を置くジョイントベンチャーであるVisionary Yike Stemcell Technologies Inc.を設立し、江蘇Yike Retic Medical Technology社と戦略的合意を締結しました。 幹細胞 研究、臨床応用、グローバル化
アジアパシフィック 細胞療法の市場 トレンド
アジア・パシフィック・セル・セラピー・マーケットは、日本のイノベーションハブとして急速に発展し、日本、中国、韓国の先進的な研究開発拠点として、強力な政府支援と広範な研究開発投資を通じて発展しています。 地域内の企業は、650以上のCGT研究で臨床試験のサージを行っています。 開発者は、セル・シート・セラピスを含む高度な再生プラットフォームを拡大し、ローカル CDMO は、成長する需要を満たし、地域全体の商業化を加速する能力をスケールアップしています。 例えば、2025年11月、ジテンドラ・シンジ大臣がインド初のシクル・セル病遺伝子治療を開始し、主に人口をターゲットとする。
アメリカ合衆国 細胞療法の市場 トレンド
米国では、「オフ・ザ・シェルフ」のカー・トゥー・プラットフォームを通じて、CDMOのエコシステムを活用し、GMP製造能力を拡大するなど、細胞療法市場を急速に拡大しています。 研究者は、最先端の遺伝子編集と細胞工学技術を応用し、新たな治療法を開発しています。 規制機関は、臨床試験活動が増加し続ける一方で、革新的な治療のための承認経路を積極的に合理化しています。 バイオテクノロジー企業、契約開発者、および病院ネットワークは、商用化を加速し、これらの治療への患者のアクセスを高めるための強力なコラボレーションを形成しています。 たとえば、8月2025日、ADIA Nutrition Inc.は、Adia Medとその高度な再生幹細胞治療をWinter Park、 Floridaのフラッグシップクリニックで発表しました。
中国・中国 細胞療法の市場 トレンド
中国細胞療法市場は、政府が強力な支持、規制当局が承認を合理化し、償還フレームワークが拡大するにつれて急速に進んでいます。 国内企業は、プロセス革新によるコストを削減しながら、自動およびアホメジックCAR-TおよびTCR療法の両方を開発しています。 上海、シンセンおよび北京のBiotechハブはGMPの製造業およびCDMOの機能のスケールをです。 同時に、企業はより多くの臨床試験を実施し、がん治療の需要が高まっています。中国はグローバル細胞療法市場での重要なプレーヤーとして確立されています。 例えば、2024年1月、Fosun Kite Biotechnologyは、治療が失敗した場合、600,000元($84,300)までのがん患者を提供する中国初の結果ベースのCAR-T細胞療法計画を開始しました。
エンドユーザーのフィードバックとアンメットは、 細胞療法の市場
- 患者のアクセスおよび耐久性: 患者および介護者は、高コスト、複雑な病院の要件、および限られた治療センターによる細胞療法へのアクセスに関する課題を頻繁に強調します。 より手頃な価格のセラピー、より広い保険のカバレッジ、専門的注入および監視センターの拡大の必要性を強調し、都市および農村地域の可用性を改善します。
- 安全および副作用管理: ヘルスケアプロバイダーは、シトカイン解放症候群や神経毒性などの治療関連の有害事象の管理に関する懸念を報告しています。 彼らは、改善された安全プロトコルの必要性を強調します, リアルタイムの監視, 標準化された管理ガイドライン 合併症を削減し、高度なセル療法で患者の自信を高めるために.
- 処置の個人化: 臨床医や研究者らは、よりパーソナライズされた細胞療法に対するアプローチの需要を示しています。 患者の遺伝学、腫瘍プロファイル、および免疫反応の違いは、個々の患者のリスクを最小限に抑えながら、有効性を最大化する予測バイオマーカーと調整された治療設計の必要性を強調しています。
細胞療法 市場動向
Allogeneicの拡張 「Off-the-Shelf」セラピー
市場は、自律から全身細胞療法へのシフトを目撃しており、複数の患者が単一のドナーソースから処理できるようにしています。 この傾向は、スケーラビリティを高め、製造時間を削減し、コストを削減します。 バイオテクノロジー企業は、ユニバーサルドナーセルと遺伝子編集技術を投資し、オフザシェルフCAR-TとTCRセラピスを作成します。 病院やCDMOは、これらの治療をサポートするためのインフラを適応させ、地域全体の品質と規制遵守を維持しながら、より迅速な患者のアクセスを可能にします。
人工知能とオートメーションの統合
AIと自動化は、細胞療法の開発、製造、臨床管理を変革しています。 AIモデルは、患者データを分析し、細胞の選択、治療の予測、臨床試験設計の合理化を最適化します。 自動化された製造システムは再現性を高め、人間の間違いを減らし、生産周期を加速します。 これらの技術は、効率性、精度、スケーラビリティを向上させます。 ステークホルダーは、AI主導の意思決定支援ツールを活用して、患者の成果を監視し、治療療法を最適化し、より良い臨床結果とより迅速な商品化を推進しています。
細胞療法 市場機会
AllogeneicおよびShelfのプラットホームの開発
患者固有の自動ログ療法からユニバーサルアソジェティックプラットフォームへのシフトは、主要な市場機会を提示します。 オフ・ザ・シェルフセラピーは、製造の複雑性を低下させ、治療時間を短縮し、スケーラビリティを拡大します。 バイオテクノロジー企業は、遺伝子の編集と免疫調節に投資し、汎用性の高い細胞を作ることができます。 病院および CDMO はモジュラー生産および自動化されたシステムを採用し、より大きい容積を処理し、アクセスを改善し、複数の患者に処置配達を同時に可能にします。
マーケットレポートスコープ
セルセラピー市場レポートカバレッジ
| レポートカバレッジ | ニュース | ||
|---|---|---|---|
| 基礎年: | 2024年(2024年) | 2025年の市場規模: | 米ドル 2,832.1 Mn |
| 履歴データ: | 2020年~2024年 | 予測期間: | 2025 へ 2032 |
| 予測期間 2025〜2032 CAGR: | 9.6% | 2032年 価値の投射: | 米ドル 5,383.4 Mn |
| 覆われる幾何学: |
| ||
| カバーされる区分: |
| ||
| 対象会社: | ブリストル・マイアーズ・スクイブ・カンパニー、アマージ株式会社、ノバルティスAG、ジラド・サイエンス株式会社、ジョンソン・アンド・ジョンソン・サービス株式会社、Allogene Therapeutics、Athersys、Inc.、Orchard Therapeutics、JW Therapeutics Co.、株式会社、Dendreon Pharmaceuticals LLC。、Autolus Therapeutics、APAC Biotech、CORESTEM、Inc.、BioCardia、Inc.、JCR Pharmaceuticals Co.、Inc.、Inc.、Inc.、Inc. | ||
| 成長の運転者: |
| ||
| 拘束と挑戦: |
| ||
75 以上のパラメータに基づいて検証されたマクロとミクロを発見: レポートにすぐにアクセス
細胞療法 マーケットニュース
- 2025年11月、ミルテンイ・バイオテックとBIRACと共同でBRIC-THSTIが、インド初のCellと遺伝子治療製造に関するトレーニングプログラムを立ち上げました。
- インドは2025年11月、病気に対する最初のCRISPRベースの遺伝子治療を開始し、大きなAtmanirbhar Bharatマイルストーンを達成し、地域、特に部族の人口に対する新たな希望を提供し、条件に不当に影響を受けています。
- 10月2025日 マイト 自動化されたCDMOを立ち上げ、再生医療の重要なボトルネックに取り組む:幹細胞由来セラピスのスケーラブルで費用対効果の高い製造。
アナリストオピニオン(エキスパートオピニオン)
- 細胞療法のセクターは重要なインフレクションポイントであるように見えます。 臨床的進歩は、2020年以降に開始された900以上のCAR T試験で、予想をはるかに超えています。 たとえば、腫瘍学に焦点を当てた2025年第1四半期に発売された79の新しい遺伝子、細胞、およびRNA療法試験の57%は、がんターゲットのアプローチにおける継続的な自信を反映しています。
- しかしながら、資本金を締める。 先進的な分子療法の90の取引は、前四半期から20%減少したQ1 2025で記録され、初期段階の資金は契約、成長した投資家の注意を促す。 高い開発コストと複雑な製造要求は、このヘシテーションに貢献することができます。
- 製造は重要なボトルネックのままです。 セルアレスなどの企業は、自動生産システムを強化していますが、フィールドは一貫性とスケーラブルなプロセスに悩まされています。 継続的な試験の多くにもかかわらず、候補者の試行は実質的であり、限られた耐久性や安全上の懸念のために多くの療法は進行に失敗しています。
- 強固な腫瘍は中央の課題になっています。 胃がんの最近のランダム化CAR T試験では、標準ケアよりも生存率が約40%向上し、奨励証拠を提供します。 しかし、血液がんで見られる成功を再現することは、固形腫瘍微分化、抗原分散性、およびT細胞排気による困難です。 二重抗原車や強化された交通戦略などのイノベーションは、初期の実証から標準のケアの実行可能性まで多くのプログラムを移行する必要があります。
- AIとメカニスティックのモデリングは、トランスフォーマーになるように表彰されます。 ターゲット発見、毒性予測、および合理的なCAR設計にマルチエージェントのAIプラットフォームを適用していますが、数学モデルは、CD4:CD8比および腫瘍空間アーキテクチャなどの要因が治療反応に影響を及ぼすのを明らかにしています。 これらのツールが成熟するにつれて、開発を加速し、プログラムリスクを削減することができます。
- 規制の不整列は、別の課題を提示します。. アナリストは、さまざまな細胞および遺伝子治療のためにFDAおよびEMAに提出された臨床データに不十分な調和を提案したことを指摘しました。 このような不整合性は、承認遅延またはブリッジング試験のための追加の要件につながる可能性があります。
- これとは別に、CAR-NK療法の急速な上昇は注目すべきです。 CD19 CAR-NKの73%応答速度など、120以上のアクティブトライアルと早期のエビデンスで、これらのセラピスはより安全で、よりスケーラブルな選択肢を提供できます。 臨床性能が改善し続ければ、CAR-NKは、特に安全・安心な製造がパラマウントされている状況において、現在のCAR Tランドスケープを著しく破壊する可能性が高まっています。
市場区分
- 治療の種類 インサイト(Revenue、USD Mn、2020 - 2032)
- 幹細胞
- Tセル
- Dendritic細胞
- NKセル
- 徴候(Revenue、USD Mn、2020 - 2032)
- 腫瘍学
- カーディオロジー
- 神経科
- その他
- エンドユーザーインサイト(Revenue、USD Mn、2020 - 2032)
- 病院
- クリニック
- 研究機関
- 地域洞察(Revenue、USD Mn、2020 - 2032)
- 北アメリカ
- アメリカ
- カナダ
- ラテンアメリカ
- ブラジル
- アルゼンチン
- メキシコ
- ラテンアメリカの残り
- ヨーロッパ
- ドイツ
- アメリカ
- スペイン
- フランス
- イタリア
- ロシア
- ヨーロッパの残り
- アジアパシフィック
- 中国・中国
- インド
- ジャパンジャパン
- オーストラリア
- 韓国
- アセアン
- アジアパシフィック
- 中東
- GCCについて 国土交通
- イスラエル
- 中東の残り
- アフリカ
- 南アフリカ
- 北アフリカ
- 中央アフリカ
- キープレーヤーの洞察
- ブリストル・マイアーズ・スクイブ・カンパニー
- 株式会社アムゲン
- ノバルティスAG
- ジャイラドサイエンス株式会社
- ジョンソン&ジョンソン 株式会社サービス
- Allogene治療薬
- アサーシス株式会社
- オーチャード治療薬
- 株式会社JWセラピューティクス
- Dendreon Pharmaceuticals LLC(デンデロン医薬品)
- オートラス治療薬
- APAC バイオテクノロジー
- CORESTEM株式会社
- バイオカード株式会社
- 株式会社JCR医薬品
- オックスフォード・バイオメディカ
- 株式会社カシ製薬
ソース
第一次研究インタビュー
- バイオテクノロジー企業(CAR-Tや幹細胞会社など)における細胞療法研究開発ヘッドへのインタビュー
- 臨床医とのディスカッション/細胞療法における臨床試験を実行している主要な研究者
- 病院ベースのGMP施設やCDMOの製造リードとの会話
- セル遺伝子治療の承認に従事する規制専門家(例、元FDA / EMAレビュースタッフ)
データベース
- ASGCT/Citeline 「Gene, Cell, + RNA」 を セラピー・ランドスケープ・レポート
- 臨床試験リポジトリ(例、臨床的trials.gov)
- 一般的な遺伝子と細胞療法パイプラインの追跡データベース(例、専門社会)
雑誌
- 自然バイオテクノロジー
- バイオセンター
- サイエンティスト
ジャーナル
- 分子療法(ASGCTのジャーナル)
- 幹細胞レポート
- 細胞療法におけるCAR-TモデリングやAIに関するPeer-reviewedプリプリント研究
新聞
- 業界を牽引する発表のためのロイター(例:武田退役細胞療法)
- ファイナンシャル・タイムズ(セルセラピーの買収など)
協会について
- 米国遺伝子治療学会(ASGCT)
- 細胞・遺伝子治療の国際社会(ISCT)
- 遺伝子と細胞療法の欧州連合(ESGCT)
パブリックドメインソース
- 計算/AI-drivenの細胞療法の研究のためのプレプリントサーバー(例えば、arXiv)
- 会議の進行/社会年次会合(例:ISCT)の抄録
- 規制機関のプレスリリース(例、FDA、EMA)
- 臨床段階の細胞療法会社(例えば、Lineage Cell Therapeutics)による企業パブリックフィリングまたは投資家プレゼンテーション
独自の要素
- ログイン データ分析ツール
- 過去8年間、CMIの既存の情報リポジトリ
著者について
Abhijeet Kale は、バイオテクノロジーおよび臨床診断分野で 5 年間の専門経験を持つ、結果重視の経営コンサルタントです。科学研究とビジネス戦略の豊富な経験を持つ Abhijeet Kale は、組織が潜在的な収益源を特定し、ひいてはクライアントの市場参入戦略を支援します。彼は、FDA および EMA の要件を満たすための堅牢な戦略をクライアントが開発できるよう支援します。
独占トレンドレポートで戦略を変革:
よくある質問