ウイルスベクターとプラズマDNA製造市場規模とシェア分析 - 2026 へ 2033
ウイルスベクターとプラズマDNA製造市場は、成長を期待しています 23.0%のCAGR お問い合わせ 米ドル 1,798.6 Mn 2026年にシェアし、到達する見込み 2033年のUSD 7,571.1 Mnお問い合わせ 遺伝子および細胞療法パイプラインのライジング(米国遺伝子治療協会(ASGCT)は、Q4 2025の1,888遺伝子治療の臨床試験がグローバルに開かれ、臨床試験活動の上昇、GMP製造ニーズの増加、およびベクトル設計および生産技術の進歩により、ウイルスベクターおよびプラシドDNA製造市場の成長を促進し、より広範な治療アプリケーションをサポートし、高度な治療薬の商用化を拡大する。
キーテイクアウト
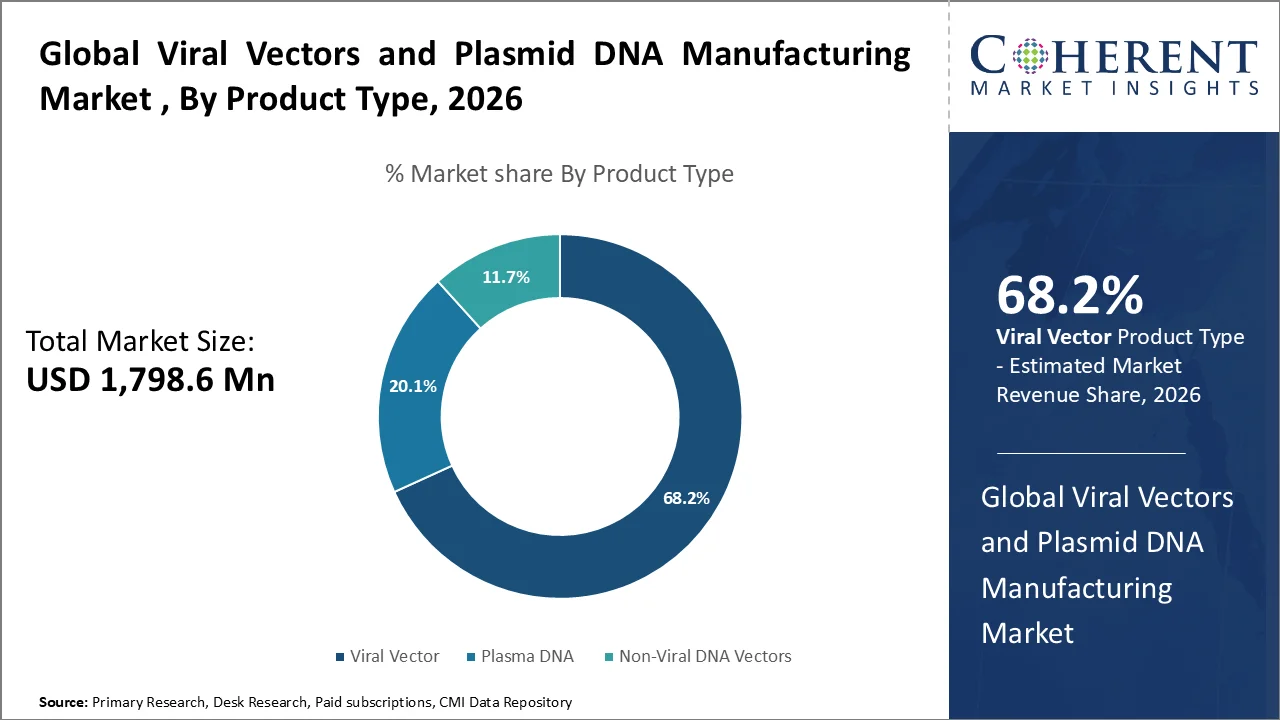
- ウイルスベクターは、その高効率、承認された治療における広範な使用、および臨床パイプラインにおける強力な存在によって駆動され、2026年に68.2%の最大のシェアを考慮することが期待されます。 例えば、2025年12月には、国立研究開発法人バイオテクノロジー情報センターが公表するデータによると、7つの新しいFDA承認ウイルスベクターベースの遺伝子治療、5 AAVベースの療法を含む。 また、アメリカ遺伝子治療学会(ASGCT)が公表したデータによると、遺伝子治療は1月2026日(遺伝子改変細胞療法を含む)で41遺伝子治療が世界的に承認されたと推定されています。
- 治療薬適用に基づいて、がんは2026年に47.5%を支配します。 細胞と遺伝子治療臨床検査の数が高まり、グローバルがんの負荷が高まります。 例えば、2026年1月、米国がん協会のがん統計2026報告書(2026年1月発行、バイオテクノロジー情報センターでアーカイブ)で公表されたデータによると、約2.11と推定されている がん新症例626,000頭のがん死亡は2026年米国で予定されている。
- 遺伝子治療は、承認済みおよびパイプライン遺伝子治療のアカウントで2026年に46.5%の優勢なシェアを保持し、ウイルスベクトル(AAV、レンチウイルス)に対する強い信頼性、および重要な投資および臨床成功率。 たとえば、Precision Medicine Group, LLC が公表したデータによると、2025年10月には、世界中で約3,200件のアクティブ遺伝子治療の臨床研究が行われ、Phase 1 と Phase 2 の何百人もの候補者と、約 35 のアプローチフェーズ 3 では、ウイルス性ベクター技術に関する重要な信頼性を示し、商用化の見通しを改善しました。 (出典: 精密加工 医学のため)
- 北米は、2026年に45.0%の優位なシェアを獲得すると予想され、主要なバイオテクノロジー企業、高度な医療および研究インフラ、および有利な規制環境の存在が強い。 例えば、2026年1月、米国食品医薬品局は、ウイルスベクターベースの製品を含む、細胞および遺伝子治療に対する化学、製造、制御(CMC)の要求に対するより柔軟なアプローチを明らかにした。 エージェンシーの改訂ポリシーは、品質基準を把握し、比較データをサポートすることで、臨床段階間の小規模な生産調整を可能にしながら、製品リリース基準を定義するメーカーの柔軟性を高めています。 この規制の柔軟性の目標は、開発をスピードアップし、新しい治療法の生産に障害を下げることです。
治験実施件数の上昇
治験の増加数が大幅にウイルスベクトルと石膏DNA製造市場成長を主導しています。 臨床試験の重要な増加 遺伝子治療 そして高度の生物的論理はウイルスのベクトルおよびplasmid DNAの製造業のための要求を高めました。 Heceは、新規創薬の臨床試験の数が増えることにより、GMPグレードのベクターとPlasmidsの需要が高まっています。 例えば、臨床治験薬(NLM)の国立図書館が公表したデータによると、2025年4月に報告した。 gov の設立 2000, 以上 573,913 臨床研究が登録されています。. 臨床Trials.govによると、, 37,597 新しい研究は、レジストリにアップロードされました 2025 単独で, 継続的な登録活動の高いレベルを実証. 異なるソースによると、7,000以上の新しい研究は、2026年にCryicalTrials.govに登録され、高年トライアル投稿パターンを維持しました。 遺伝子治療(79)と非遺伝子改変細胞治療(29)を組み合わせた2026に登録された約106件の新試験が新たに登録されています。
政府の支援と有利な規制法の強化
有利な政府の支援と規制は、近い将来にウイルスベクターとプラシドDNA製造市場の成長のための重要な機会を作成すると推定されています。 バイオ医薬品のイノベーションと製造インフラの推進に関する方針は、バイラル・ベクターとプラシドDNA製造市場の需要を主導しています。 規制当局の承認を増加させ、ウイルスベクターとプラシドDNAの商品化を促す。
- たとえば、2026年1月、米国食品医薬品局は、遺伝子および細胞治療に関する化学、製造、制御(CMC)の規制を管理するためのより十分なアプローチを確認しました。 この柔軟性は、特に、製品開発をスピードアップし、BLAアプリケーションをより簡単にし、ウイルスベクターベースの医薬品および関連する製造プロセスの革新をサポートすることを意図しています。
- さらに、2026年2月、米国食品医薬品局は、非常にまれな病気のためにカスタマイズされた遺伝子およびRNAベースの治療のための安全性と有効性の強い証拠を作り出すための新しい規制枠組みを概説するガイドラインを発表しました。 小さな患者グループがランダムに制御された試験を実用的に行なうと、パラダイムは、これらの調整された治療の承認を正当化しようとします。 スポンサーは、特定の遺伝的、細胞的、または明らかに医学的徴候に関連する分子的収差を識別するために、フレームワークによって必要です。 また、スポンサーは、具体的に基礎的または近隣の有害な生物学的変化に対処する処置を作成しなければなりません。 提案されたガイダンスによると、このメソッドを使用して生成されたエビデンスは、現在の規制プロセスの下でライセンスまたは承認を正当化するのに十分であるかもしれません。 製品の安全性、有効性、品質を証明するために、代理店は、適切な非臨床的、臨床的、化学的、製造、および制御(CMC)データの必要性を強調した。
長期拡張 用語集製造 パートナーシップ:バイラルベクターとプラシドDNA製造における主要な画期的な
パートナーシップやコラボレーションなどの無機成長戦略の採用を増加させ、新しい遺伝子治療の開発のためのプラシドとウイルスベクトルの製造を加速しました。 まれで慢性的な病気を治療することを目的としたものを含む遺伝子治療の増殖は、ウイルス性ベクトルと石膏DNA製造市場規模の第一次的要因の一つです。
- たとえば、2026年3月には、バイオテクノロジー、栄養、医薬品市場向けのグローバル・コントラクト開発・製造機関(CDMO)のLonzaは、商業段階のバイオテクノロジー会社であるGenetix Biotherapeutics Inc.(Genetix)とパートナーシップを結び、長期的な商用製造契約の延長を発表しました。 GenetixのZYNTEGLOの需要増加を満たすためには、輸液依存のベータ血症の成人および小児患者のための唯一のFDA承認遺伝子治療、Lonzaは、拡大された合意の下で製造能力を高めます。
ソース: ロンザ
現在のイベントとウイルスベクターとプラシドDNA製造市場への影響
現在のイベント | 説明とその影響 |
有利な規制方針の拡大 |
|
政府の支援増大 遺伝子と細胞療法の成長 |
|
75 以上のパラメータに基づいて検証されたマクロとミクロを発見: レポートにすぐにアクセス
なぜウイルスベクターが最大の市場シェアを買収するのですか?
ウイルスベクターは、2026年にウイルスベクターとプラシミドDNA製造の最大のシェアを占め、合計ボリュームの約68.2%を表しています。 ほとんどの市販の遺伝子治療はウイルス性ベクトル(AAV、レンチウイルス)に依存しています。 大規模な製造要求を直接駆動します。 ウイルスベクターは、高透過効率(遺伝子を細胞に非常に効果的に届ける)を持っています。 プラスミドDNAと非ウイルス系と比較して、より信頼性が高い。 遺伝子および細胞療法の進行中の臨床試験の大規模なシェアはウイルスベクトルを使用します。 これは、近い将来に持続的な需要を確保します。 ウイルスベクターは、CAR-T特にレンチラルベクターのような細胞療法で広く使用されています。 これらの治療法は、腫瘍学に急速に拡大しています。 ウイルスベクターベースの製品は、より規制当局の承認とより明確に定義されたGMP製造プロセスを持っています。 これらは成熟性の利点を与えます。 ウイルスベクターは複雑で高価な製品です。 小さなボリュームでも、石膏DNAと比較して高い収益シェアを生成します。 資金調達とコラボレーションの増加は、バイラルベクター生産能力拡大に重点を置いています。 多くのCDMOは、ウイルスベクトル製造を専門としています。 製造精度とターゲティングセラピスにおけるバイラルベクターの需要は、市場でのセグメントの優位性をサポートしました。
- 例えば、2026年3月、米国に拠点を置くSK pharmteco Inc.は、バイラル・ベクター事業を通じた機能強化と増大を発表し、SK Pharmtecoは100万ドルを投資しています。 これは、主に、コルビル・エソンズ、フランス、そしてPrussiaの王、ペンシルバニア州で卓越性の会社のセンターに影響を与えます。 柔軟なCDMOであることは、SK Pharmtecoによると、バイオファーマ事業は、確立された治療から革新的な治療に至るまで、さまざまなパイプラインを作成します。
がんは最大の市場シェアを保持
治療アプリケーションに基づいて、がんは市場を支配し、2026年に有意な47.5%の株式を占め、癌に焦点を当てた遺伝子治療臨床試験の重要なシェアを借ります。 がん治療の開発に重点を置いた臨床試験により、ベクターとプラシドミド製造の需要が高まっています。 世界中のがんの発生を増加させ、革新的な治療の必要性を運転しています。 これは、腫瘍学における投資および製品開発を強化します。 免疫腫瘍学および遺伝子修飾された免疫細胞および腫瘍性ウイルスの進歩の高度の革新は区分の優位性を支えました。 これらのアプローチは、ウイルスのベクトルと石膏のDNAに依存しています。 がん研究は、政府やバイオテクノロジー企業から大幅な資金調達を受けています。 研究開発・生産ニーズを加速します。 たとえば、がん予防、検出、治療の進歩を加速する努力で、世界的ながん研究は、1926年4月26日、最先端の研究プロジェクトで資金調達を発表しました。 これらの取り組みは、高リスク、高報酬の概念に焦点を合わせた「キュアスターター」(サポーターや研究者)が、最終的に治療を発見する努力によって急上昇しています。 国際的に提出されたアプリケーションから選択されます。
どの製品セグメントが市場を支配しますか?
このレポートについてもっと知りたい方は, 無料サンプルをダウンロード
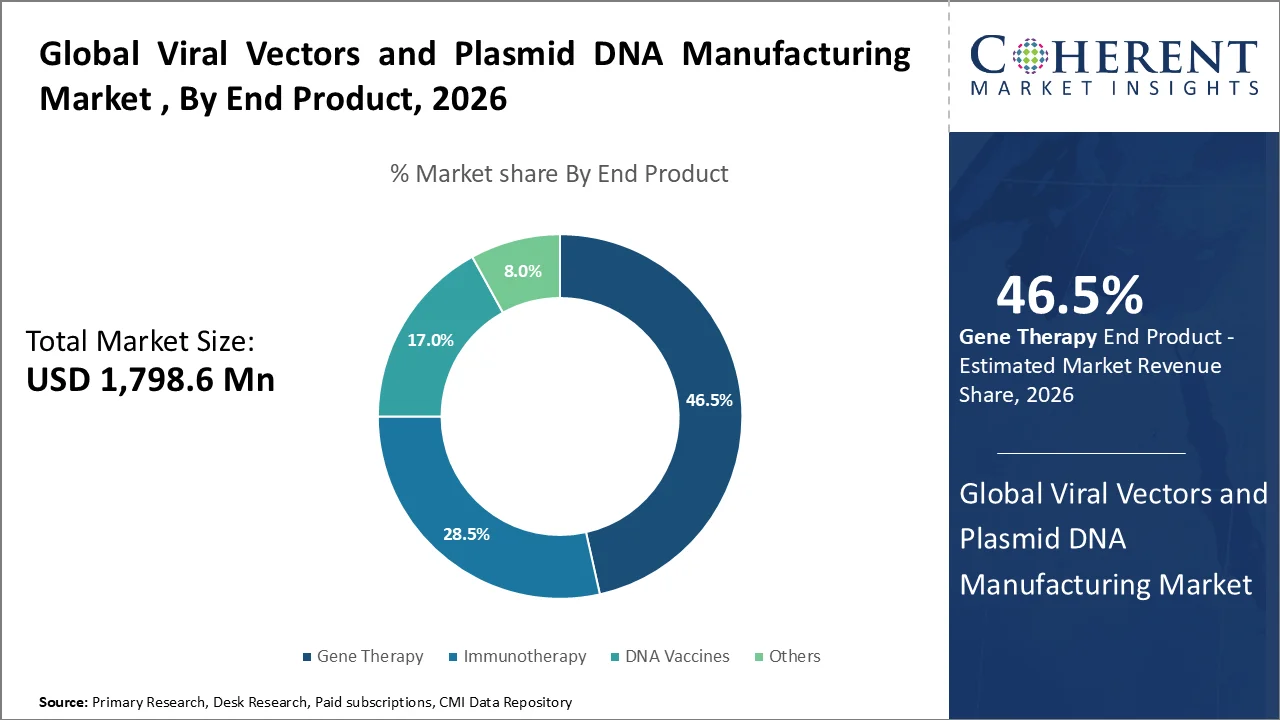
遺伝子治療は、2026年に最大46.5%の割合で、ウイルス性ベクターや石膏DNAに対する高い信頼性と承認された治療の数の増加によるものです。 遺伝子治療は、遺伝子配信のためのウイルスベクトル(AAV、レンチウイルス)に直接依存します。 プラシド DNA は、ベクター生産の開始材料としても広く使用されています。 まれな遺伝障害および特定の癌のための遺伝子療法の承認の増加。 大規模な製造業の需要を促進します。 継続的な臨床試験の大きな比率は、継続的かつ長期的要求を保証する遺伝子治療に焦点を当てています。
たとえば、2026年、国立研究開発法人国立研究開発法人 バイオテクノロジー情報センターが公表したデータによると、2026年初頭に世界規模で3,900以上の研究と2,150以上の治療が急速に成長していると推定されています。 2026年、米国FDAの処理に集中し、VIVO遺伝子治療(サイレンバイオテクノロジー)の先進的な研究とINDを提出する。 AIの統合と分散型試験モデルは重要な傾向であり、細胞と遺伝子治療の市場は2035年までに飛躍的に拡大することが期待されます。 さらに、2026年3月、米国食品医薬品局は、Kresladi(marnetegragene autotemcel)の認可を明らかにし、重度の白血球粘度欠乏症型I(LAD-I)のための最初の遺伝子治療を明らかにしました。 人間の白血球の抗原(HLA)に一致させた兄弟のドナーが全身の hematopoietic 幹細胞の移植のために利用できなければ、Kresladi は重度の白血球の付着の deficit I (LAD-I) の juvenile の患者の処置のために推薦されます。
ウイルスベクターとプラシドDNA製造市場動向
- AAVおよびLentiviralのベクトルの上昇の焦点: AAVおよびlentiviralベクトルの上昇の焦点はウイルスベクトルおよびplasmid DNAの製造業の要求を運転しました。 安全・精度でAAVベクターを支配します。 レンティビアルベクターは、CAR-T療法で使用するため急速に成長しています。
- 患者固有の療法の成長: 患者固有の治療の成長、特に腫瘍学ドライブでは、カスタマイズされた、小ロットの製造が必要です。
- 製造業の拡大 容量: 製造業の容量の拡大は近い将来市場の成長をかなり運転しました。 企業は、グローバルな需要を増加させるために、新しい設備とモジュラー製造ユニットに投資しています。 たとえば、11月2025日、ノバルティスは、革新的な医薬品の製造に焦点を当てた会社で、エンドツーエンドの生産能力を備えた新しいフラッグシップ製造ハブは、計画に応じてノースカロライナに設立されます。 戦略的投資は、米国の患者のためのすべての重要なノバルティス薬が国内で生産され、大規模に全国の患者に配布されていることを確実にするための重要なステップです。
- この発表は、Novatisの米国ベースのインフラの次の5年間で23億ドルの投資のコンポーネントであり、生産能力を高め、米国で完全に生産されるすべての企業の主要な薬のためにそれを可能にすることを目指しています。さらに、1月2026日、米国食品医薬品局(FDA)は、Seren Biotechnologyの第一次Inveigational New Drug(IND)アプリケーションを承認し、同社が最初の臨床試験を開始できるようにしました。 サイレンバイオテクノロジーは、ユニバーサルAAV免疫遺伝子治療のパイオニアです。 この承認により、サイレンは臨床段階におけるバイオテクノロジー企業となります。
出典:ノバルティス
- パーソナライズされた医学のための上昇の要求: ウイルス性ベクターおよび石膏DNA製造市場成長を主導する個人化された薬のための上昇の要求。 患者固有の治療の成長、特に腫瘍学ドライブでは、カスタマイズされた、小ロットの製造が必要です。 たとえば、2026年4月、バイエルAGの医薬品部門長、経営委員会のメンバーであるステファン・オエルリッチは、バイエルのファーマ・メディア・デイ2026の機会に2030に向かって予測された成長軌跡を、科学とビジネスの優先順位に重点を置いた方法について議論しました。 さらに、2026年に、Gileadの科学、製薬会社は個人化されたYescartaの製造業を拡大しました CAR-T療法 カリフォルニア・フォスター市に新施設で先進的なウイルスベクター技術を取り入れ、がんのために。 患者固有の医薬品の増大の必要性を満たすために構築されたこの施設によってカスタマイズされた小さなバッチ生産が可能です。
ソース: バイエル
- エンドツーエンド製造の統合 ソリューション: エンドツーエンド製造ソリューションの統合は、市場の成長のための重要な機会を持っています。 企業は、Plasmid DNA、ウイルスベクターから最終製品までフルサービスプラットフォームを提供し、効率性を高め、タイムラインを削減します。 たとえば、2024年10月、ロンザグループAG、製造会社では、バイオ医薬品産業の支援を計画し、細胞や遺伝子治療に重点を置いています。 オランダのジェリーンに新たな生産設備の確立により、大規模に複雑なバイオロジックを作成する同社の能力が向上します。 ヘルスケア業界における新規治療の必要性を満たすため、最先端の技術を駆使して生産手順を最適化します。
地域洞察
このレポートについてもっと知りたい方は, 無料サンプルをダウンロード
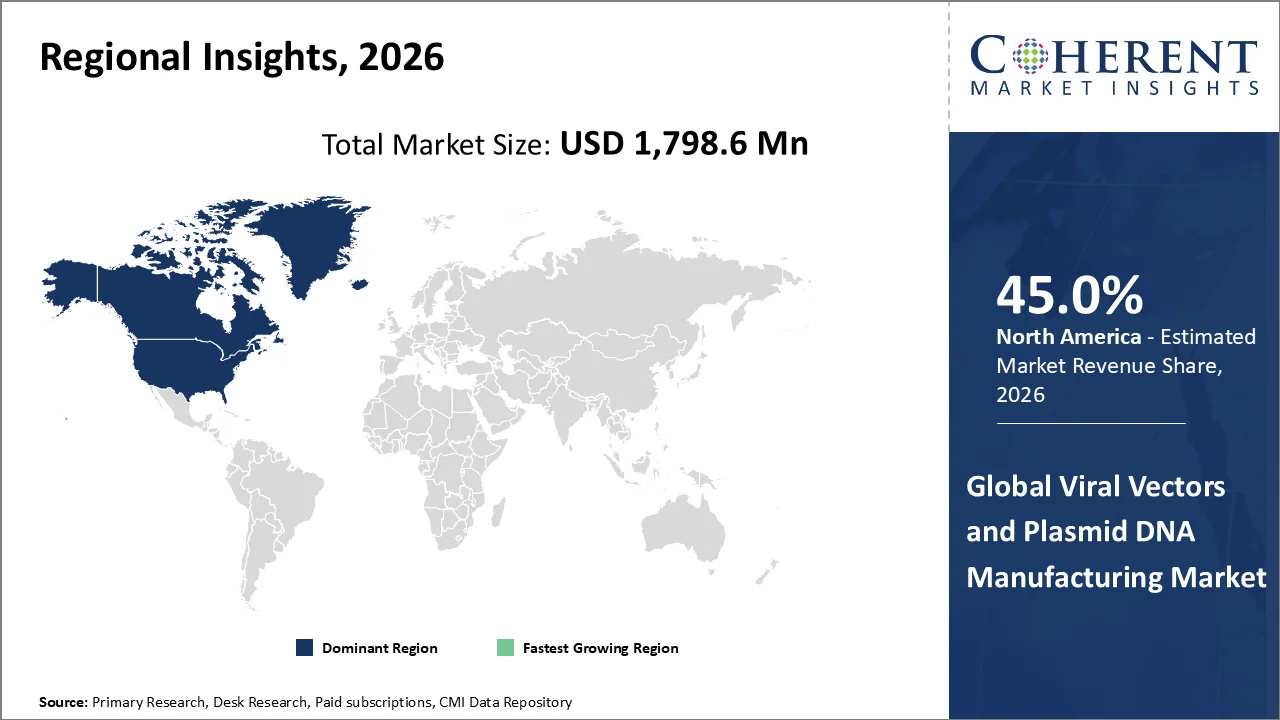
北米は、好ましい規制環境と研究インフラに恵まれています
北アメリカのアカウント 45.0% 市場シェア 2026, 有利な規制環境と重要な資金と投資によってサポート. 北米は、主要な遺伝子治療の開発者やベクターメーカーが、ウイルス性ベクターとプラシミド DNA の高かつ一貫した需要を生み出しています。 北米の先進医療・研究インフラと、最先端のバイオ医薬品エコシステム、GMP施設、研究ラボでは、大規模かつ高品質な製造が可能です。 北米地域(特に米国)は、世界的な遺伝子治療臨床試験の大きなシェアを占めています。 レギュレーションボディはより速い開発および商品化を促進する高度の療法のための明確な指針そして速いトラックの承認を提供します。 たとえば、2025年4月、サーモフィッシャーサイエンス株式会社、科学および臨床研究会社では、同社が次の4年間に米国に2億米ドルを投資し、アメリカの製造、イノベーション、および生命科学業界における経済競争力を高めます。 世界最大の医薬品メーカーであるサーモフィッシャーは、バイオ医薬品事業が米国で製品を製造・製造することを可能にします。 堅牢な米国医療サプライチェーンは、米国のアメリカの製造能力におけるこれらの新しい投資によってサポートされています。これにより、アメリカの経済全体で重要なマルチプライヤー効果が得られます。 次の4年間で、USD 2億の投資は以下のとおりです。
米国の製造業の操業を改善し、成長するために資本支出のUSD 1.5億
高インパクトイノベーションに重点を置いた研究開発で500万ドルの投資
アジア・パシフィック・バイラル・ベクターとPlasmid DNA製造市場動向
アジア・パシフィック地域は、2026-2033年までに急速に成長する地域として表彰され、慢性疾患および遺伝疾患の普及が進んでいます。 遺伝子障害、がん、感染性疾患の増大症は、アジア太平洋地域におけるウイルス性ベクターおよび白質DNA製造市場の需要を主導しています。 たとえば、2026年に、国立研究開発法人バイオテクノロジー情報センターが公表したデータによると、アジアの人口は毎年、がんと診断され、アジア太平洋地域で最もよくある病気になります。 世界各地のがん症例の49%で、アジアはがんの負担が最も高く、地域の労働力と公衆衛生問題の上昇を強調しています。
また、アジア太平洋地域の政府機関は、規制改革、資金調達プログラム、国家ミッション(バイオ医薬品イニシアティブなど)を通じてバイオテクノロジーを推進しています。 これらの方針は製造業および革新を加速します。 たとえば、2026年2月、インド政府の記者情報局が公表したデータによると、インドの医薬品に対するアプローチは、その生産と医療戦略の核となるバイオ医薬品とバイオ医薬品を配置する連合予算2026〜2027と大きな変化を遂げていると説明しました。 インド政府が世界規模のバイオ医薬品業界においてインドを主要なプレーヤーにし、世界市場の5%を占めるという目標を達成しています。 Biopharmaの進水 SHAKTIは、インドのエンドツーエンドの生態学とバイオシミラーのエコシステムを改善するためにコミットされた国家プロジェクトで、Rs.を5年以上費やす。 イニシアチブの目標は、国際バイオ医薬品サプライチェーンにおけるインドの競争力を高めることであり、輸入に関する信頼性を低下させ、高付加価値バイオ医薬品および医薬品の国内発見と生産を促進することです。 医薬品教育研究機構(NIPERS)の3つの新国立研究開発法人を設立し、バイオ医薬品を中心としたネットワークの整備・強化・拡充を進めています。 この提案は、バイオ医薬品の製造、研究、開発、規制における高度に専門的人材の必要性に対処することを目指しています。
先進的な研究開発とヘルスケアインフラは、米国におけるバイラル・ベクターとプラズマミドDNA製造市場需要を加速
米国のバイラルベクターと石膏DNA製造市場は、堅牢な拡張の期間を経ています。 米国の国では、大学や研究センターが、分子生物学や遺伝子の編集に積極的に取り組んでいます。 また、アウトソーシングやスケーラビリティをサポートする多くの専門契約製造機関があります。 NIH、ベンチャーキャピタル、民間バイオテクノロジー会社などの米国政府機関からの強力な財務支援により、イノベーションと能力の拡大を推進しています。 たとえば、2026年2月では、プラットフォームベクター遺伝子治療(PaVe-GT)の取り組みは、同AAV配信システムと複数のプログラムを横断する製造技術を利用して、希少疾患遺伝子治療の有効性を高めることを目的としており、国立衛生研究所(NCATS)の先進的翻訳科学センターが強調した。 また、NCATSは、遺伝子治療の創造と分布を明示するために標準とプラットフォームを作成することを目的としたパブリックプライベートなコラボレーションであるBespoke Gene Therapy Consortium(BGTC)のリーダーシップに関与すると主張しています。 同時に、米国FDAは、遺伝子および細胞療法に対する化学、製造、制御(CMC)の規制が製品開発を加速し、より迅速な商品化を促進するために期待されていると述べた。 これらの進歩は、堅牢な米国研究機関、政府主催のイニシアチブ、および規制の裏付けが、白中DNAおよびウイルスベクトルにおけるイノベーションとスケールの生産を推進しているかを示しています。
中国ウイルスベクターとプラズマDNA製造市場動向
中国のウイルス性ベクターと石膏DNA製造市場は、今後数年の間に著しく成長するように計画しました。 中国は急速に成長するバイオテクノロジーおよび製薬産業を持っています。 遺伝子治療やベクター生産に関わる企業が増えています。 契約開発・製造機関の急速な成長 - CDMOはサプライチェーンと生産能力を強化します。 また、中国は、国際・国内のアウトソーシングを兼ね備えた欧米諸国に比べて運用コストを削減しています。 たとえば、2026年3月、AstraZeneca plc、製薬会社では、2030年までに中国で15億ドルの投資計画を明らかにし、生産、研究、開発の能力を高めました。 この戦略は、上海のセルセラピー製造と供給拠点およびイノベーションセンターの構築を含みます。 この施設は、CAR-Tセル療法を含む最先端の治療製品の生産をサポートすることにより、複雑なバイオロジカルと遺伝子ベースの治療のための中国のバイオテクノロジーサプライチェーンとローカル製造能力を高めます。
バイラルベクターとプラシドDNA製造市場における主要企業
ロンザグループAG、FinVector Vision Therapies、Cobra Biologics and Pharmaceutical Services、Sigma-Aldrich Co. LLC、VGXI、Inc.、VIROVEK、SIRION Biotech GmbH、FUJIFILM Diosynth Biotechnologies U.S.A.、Sanofi、Cell、Gene Therapy Catapult、Brammer Bio、MassBiologics。
ニュース
- で 4月 2026, ウイルスベクターの生産のためのウイルスセシタイザー(VSE)を専門とするセルエンハンサー会社であるVirica Biotech(以下Virica)は、カナダの産業研究支援プログラム(NRC IRAP)の国家研究評議会から資金と諮問サービスを受けていると発表しました。 世界中の学術的および商業的AAVメーカーを支援するため、パートナーシップは、FUJIFILM Biosciences BalanCD HEK293媒体のVSE製剤の精製に集中します。
- 3月2026日, ニューイングランドBiolabs, Inc., ライフサイエンス会社は、英国に拠点を置くタッチライト、バイオテクノロジー会社と共同署名し、EnClose Cell-free dbDNA Synthesis Kitを革新し、発売しました。 この革新的なキットは、さまざまな核酸処理の生成において、Touchlightの排他的なDoggyboneTM DNA(dbDNA)のベンチトップ酵素合成を可能にします。
- 2月2025日, Novartis AG, 革新的な医薬品会社, 欧州全域でセルと遺伝子治療能力を向上させるためのより大きな計画の一環として、, ノバルティスは、正式に設立しました €40 百万 (US $ 41.2 百万) メンゲスロベニア州メンゲスにウイルスベクトル生産工場. VIFA Oneと呼ばれる施設は、同社の初期の試みで、大陸のウイルスベクトルを生成します。
ヴィファ・ノヴェリシスのビルは、2023年にスタートした以来、工場を最新鋭の完全自動化サイトとして位置付けました。 ウイルスベクトルの製造における生産性を高めるために、ロボティクスは1つの場所でプロセスのすべてのステップを監督します。 この成長に伴い、ノバルティスは、スロベニア州に投資する€3.5億(US $ 3.6億)を増加しました。
マーケットレポートスコープ
ウイルスベクターとプラシドDNA製造市場レポートカバレッジ
| レポートカバレッジ | ニュース | ||
|---|---|---|---|
| 基礎年: | 2025年 | 2026年の市場規模: | 米ドル 1,798.6 Mn |
| 履歴データ: | 2020年~2024年 | 予測期間: | 2026 へ 2033 |
| 予測期間 2026〜2033 CAGR: | 23.0%の | 2033年 価値の投射: | 米ドル 7,571.1 Mn |
| 覆われる幾何学: |
| ||
| カバーされる区分: |
| ||
| 対象会社: | ロンザグループAG、FinVector Vision Therapies、Cobra Biologics and Pharmaceutical Services、Sigma-Aldrich Co. LLC、VGXI、Inc.、VIROVEK、SIRION Biotech GmbH、FUJIFILM Diosynth Biotechnologies U.S.A.、Sanofi、Cell、Gene Therapy Catapult、Brammer Bio、MassBiologics。 | ||
75 以上のパラメータに基づいて検証されたマクロとミクロを発見: レポートにすぐにアクセス
アナリストオピニオン
- 市場見通しは強いままですが、価値創造は、科学的な革新だけでなく、製造の信頼性に依存します。 FDAは、製造変更、比較可能性、効力保証、および小規模な人口試験設計に関するガイダンスを含む、細胞および遺伝子治療ガイダンスフレームワークを拡大し続けています。これにより、一貫性と制御に対する規制の期待が高まっています。 その結果、企業は、強力なCMC、分析、スケールアップ機能を備えた統合開発対商業製造サポートを提供することができる最も有益です。
- ウイルスベクターとプラシドDNA 市場は、短期的なハイプではなく、構造的治療需要によって駆動されています。 Q4 2025によって、41遺伝子治療は既にグローバルに承認され、1,888遺伝子治療臨床試験が開いており、ウイルス性ベクトルおよび白中DNAに対する要求は、まれな疾患、腫瘍学、その他の高値表示に及ぶ深い臨床および商業パイプラインによって支えられています。
- プラスミドDNAは、単なる支持原料ではありません。市場向けの戦略的製造バックボーンとなっています。 FDA の指導は、DNA プラシドの中間体が AAV や lentiviral ベクトルなどの遺伝子治療製品の製造に使用されていることを明示的に指摘していますが、業界ガイダンスの作業は、細胞および遺伝子治療の生産のための重要な開始材料として plasmids に焦点を当てています。 これは、強力なプラシド品質システム、リリース仕様、およびスケーラブルなGMP容量を持つサプライヤーが、より強力な競争力を得る可能性があることを意味します。
著者について
Nikhilesh Ravindra Patel は、8 年以上のコンサルティング経験を持つシニア コンサルタントです。市場予測、市場インサイト、トレンドと機会の特定に優れています。市場動向に対する深い理解と成長分野を正確に特定する能力により、情報に基づいたビジネス上の意思決定をクライアントに導く上で、彼は非常に貴重な存在となっています。レポートを通じて、市場情報、ビジネス情報、競合情報サービスを提供する上で重要な役割を果たしています。
独占トレンドレポートで戦略を変革:
よくある質問