Humira Biosimilar市場分析と予測: 2025-2032
Humiraバイオシミラー 市場は価値があると推定される 1 成人 2 成人 3 成人 4 成人 5 成人 6 成人 7 成人 8 成人 9 成人 10 成人 2025年、到達見込み 米ドル 7,724.0 Mn 2032年、化合物の年間成長率を展示 (CAGR)の 25.9%2025年~2032年
キーテイクアウト
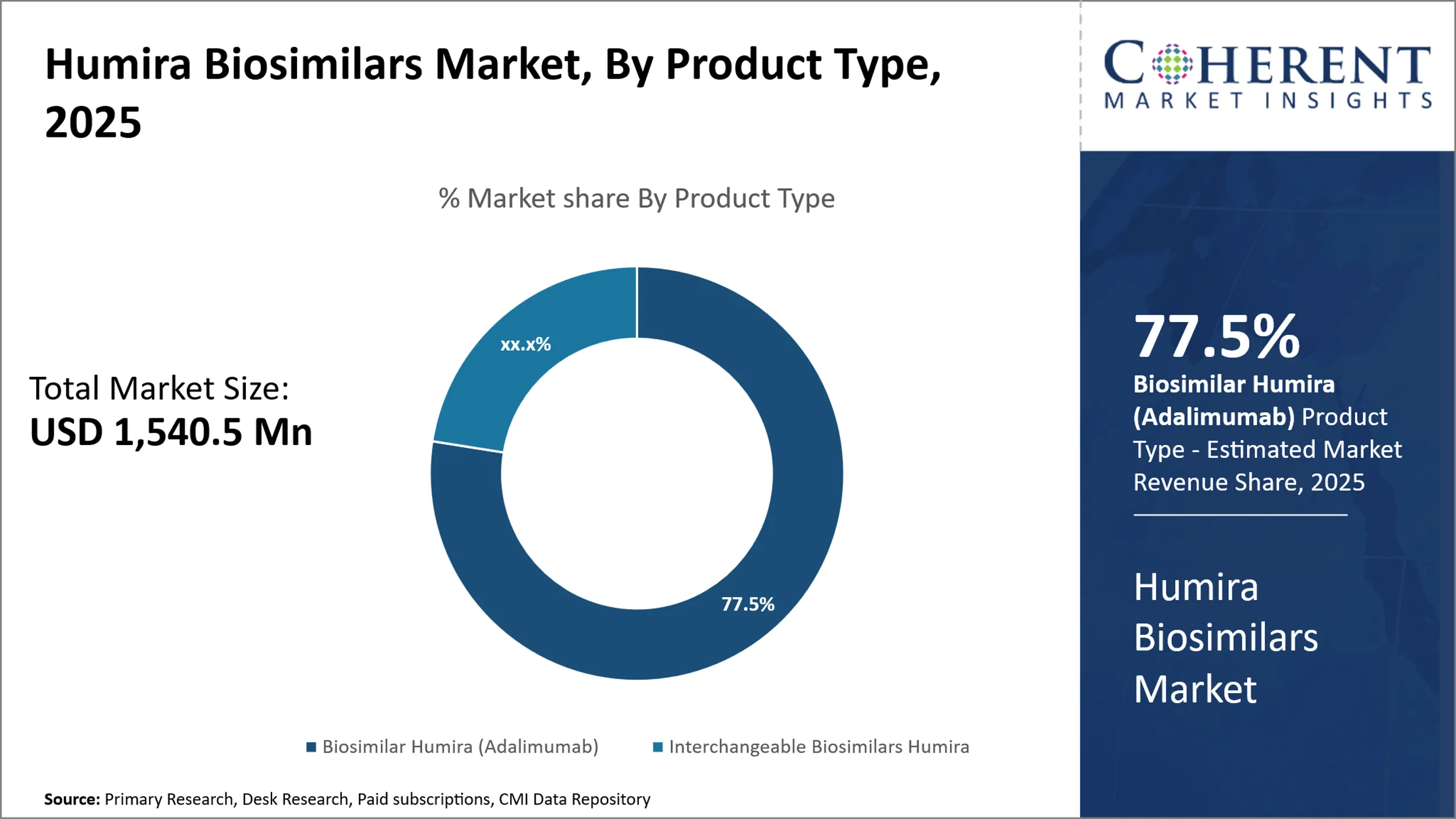
- 製品の種類によって、Biosimilar Humiraセグメントは、2025年までに有意な33.5%の市場シェアを持つ世界的なHumiraバイオシミラー市場をリードする予定です。
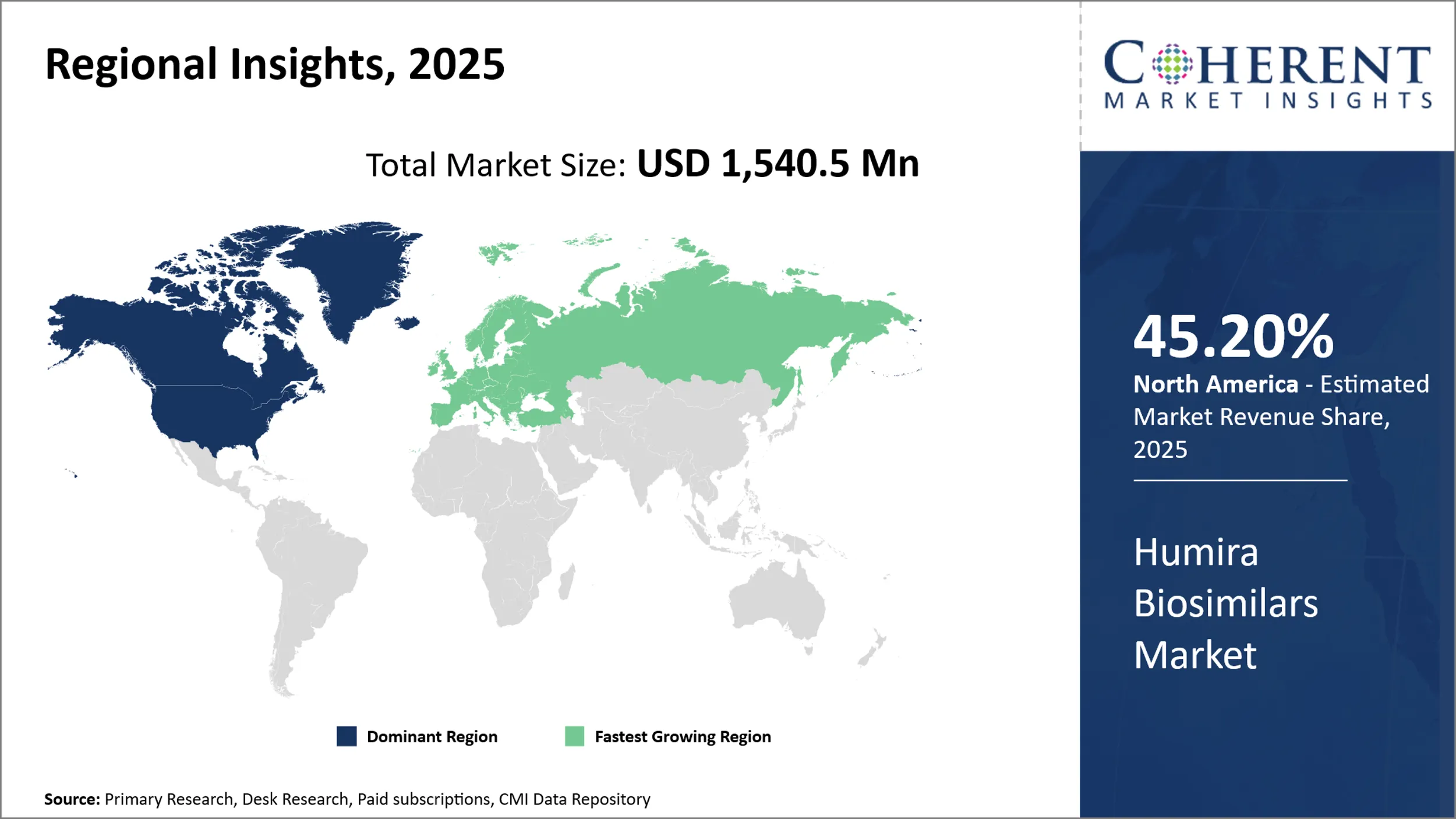
- 北米は、2025年に最大45.2%の地域シェアを持たせる見込みです。
- ヨーロッパは、バイオシミラーの採用で世界的な先駆者であり、2025年のグローバル市場シェアの約30.7%を捕捉することを期待しています。
- アジア太平洋地域は、2025年の市場シェアの約16.8%を占める急激な拡大に注目されています。
市場概観
自己免疫疾患を治療するための市場での元のHumira薬への低コストの代替のための需要のサージは、2024年に世界中のAmjevitaバイオシミラーを発売したAmgenの充填をスパイクしています。 バイオシミラーの認知度を高め、多数の特許の普及は市場成長を促進しています。 しかし、規制障害や医師の受入率は採用率を低下させる可能性があります。
Humiraはさまざまな自己免疫疾患を扱うのに使用される生物的薬物です、を含む関節リウマチそして、乾癬は、世界トップセラーの生物学的薬物であることの区別を保持し、年間売上高は20億米ドルを超える。
現在のイベントとヒマラバイオシミラー市場への影響
イベント | 記述および影響 |
米国特許クリフと市場参入タイムライン |
|
欧州バイオシミラー市場成熟と価格のダイナミクス |
|
中国バイオシミラー規制改革と市場アクセス |
|
75 以上のパラメータに基づいて検証されたマクロとミクロを発見: レポートにすぐにアクセス
価格分析
世界的なHumiraバイオシミラー市場は、特許調査、規制環境、医療システムによって形作られた多様な地域固有の価格変動を提示します。 米国では、バイオシミラーエントリー(2023)を遅らせ、複雑な保険枠組みは多面的な価格設定風景を作成します。 AmjevitaやCyltezoなどのバイオシミラーは、$ 5,500と$ 6,240の間で毎月の料金をリストします。 リベート後、ネット価格が40-60%に下がりますが、患者様は、カバレッジに基づいて大きく異なります。
欧州連合では、以前のバイオシミラーの採用(2018-2019)と集中的な調達は、国やブランドに応じて€1,100から€1,600の範囲で毎月のコストで、より競争力のある価格を主導しています。 ドイツは、交渉された割引から英国やイタリアのような市場が利益を伴って、より高い端にある傾向があります。
アジア太平洋地域は、積極的なバイオシミラーの価格設定で、重要な価格感度を展示しています。 たとえば、インドでは、Exemptia は $800-$1,200 の月間価格です。APAC 市場は最大 $2,200 の月間価格を示しています。
全体的に、バイオシミラーの価格設定戦略は、手頃な価格と市場の浸透を強調していますが、実際のエンドユーザーコストは、ローカルの払い戻しと保険要因に大きく依存しています。
Humira Biosimilar MarketでAIのような技術の役割
人工知能(AI)は、開発・製造・患者管理を強化し、ヒマラバイオシミラー市場を変革する バイオロジック セラピス 競争がヒマラバイオシミラーのような薬の間で激化するにつれて、AI主導のイノベーションは、厳格な規制基準を満たし、一貫した有効性を提供する高品質のヒマラバイオシミラー処方を確実にするために不可欠です。
AIインテグレーションは、フミラバイオシミラー処方の開発タイムラインを加速しています。 たとえば、Amgenのような大手メーカーは、機械学習アルゴリズムを使用して分子設計を最適化し、バイオシミラリティの成果を予測し、妥協することなく開発時間を約10〜5〜7年削減します。 この効率は、慢性疾患などの慢性疾患の費用対効果の高い治療法の早期参入を可能にし、安定したヒマラバイオシミラー市場成長をサポートします。
製造業では、AI による予測分析により、複雑なタンパク質のフォールディングプロセスを監視し、生産の偏差を最小限に抑え、廃棄物を減らし、バッチの一貫性を改善することにより、リアルタイムの品質管理が可能になります。 さらに、多様なHumiraバイオシミラー製品における有害事象を効果的に監視することにより、AIの強化薬理士プラットフォームが患者の安全を強化します。
患者ケアフロントでは、AI主導のデジタルヘルスツールは、付着力パターンと臨床データを分析することで治療をパーソナライズし、結果を改善し、入院を削減します。 AI技術が進歩するにつれて、現実世界証拠生成と規制プロセスにおけるその役割は、Humiraバイオシミラー市場における生態学療法の成長とアクセシビリティを強化します。
エンドユーザーフィードバック
多様なエンドユーザーからのフィードバックは、複数のセクターにわたってHumiraバイオシミラーの成長した受諾と利点を強調しています。 IVFクリニックは、予防接種治療において、自己免疫条件をサポートする費用対効果の高いバイオシミラー療法の可用性を高く評価し、介護の質を損なうことなく、全体的な患者費を削減します。
バイオテクノロジーと製薬会社は、治療ポートフォリオを拡大し、競争力のある価格モデルを有効にして、Humiraバイオシミラーの戦略的価値を強調しています。 彼らはまた、バイオシミラーは、アクセス可能な生物学的代替手段を提供することにより、研究のコラボレーションと共同開発イニシアティブを容易にすることに注意してください。
研究・学術機関は、質の高いHumiraへのアクセスの改善から恩恵を受ける バイオシミラー 慢性疾患の慢性関節リウマチなどの臨床試験および翻訳研究のための処方。 研究者は、バイオシミラーの比較可能な有効性を元のバイオロジックに報告することで、より柔軟な研究設計とコスト削減を実現します。
バイオバンクは、バイオシミラー治療患者のサンプルを含む価値を、より包括的な現実の証拠とバイオマーカーの発見のために見つける。 バイオシミラーデータの統合により、レトロスペクティブ分析の範囲を高め、パーソナライズされた医薬品の努力をサポートします。
全体的に、エンドユーザーは治療および研究の適用を渡る臨床信任を維持している間、手頃な価格およびより広い忍耐強いアクセスを運転するための安定したヒマラバイオシミラーの市場成長を表彰します。
Global Humira Biosimilar Market Insights(製品タイプ別)
製品の種類によって、バイオシミラーHumiraセグメントは、2025年に33.5%のコマンドシェアでグローバルHumiraバイオシミラー市場をリードすることが期待されます。 この主要な位置は、特にバイオシミラーのための強力な規制サポートを持つ地域で、元のヒマラバイオロジックへの費用対効果の高い代替の採用の増加によって駆動されます。
バイオシミラーセグメントは、医療提供者とバイオシミラーの比較効果と安全プロファイルに関する患者の間で成長意識から恩恵を受けており、リューマノイド関節炎や乾癬などの慢性的な条件に好まれています。
元のHumiraの区分は、まだ重要な間、特許のexpirationsおよび競争の価格設定圧力からの挑戦に直面します、生物類似体のアップテークを加速します。 しかし、その確立されたブランドの存在と広範な臨床データは、いくつかの市場で安定した需要をサポートし続ける。
新規処方または次世代の生成 製品は、代替配送方法や強化された有効性を通じて、患者の利便性を向上させることを目指し、革新によって駆動される市場にも貢献しています。 現在、小数の株式を保有しているが、予想期間を経つと予想しています。
その他のカテゴリには、さまざまな補助製品とオフラベルバイオシミラーの使用、ニッチ治療用途や地域の好みに対応できます。
地域洞察
このレポートについてもっと知りたい方は, 無料サンプルをダウンロード
北アメリカ Humira Biosimilar 市場分析とトレンド
北米は、2025年にグローバルフミラバイオシミラー市場の45.20%シェアを誇る米国によって主に主導しました。 この地域のバイオシミラーの導入は、特許保護と複雑な規制枠組みによる初期の課題に直面していますが、Humiraの特許の普及は重要な成長機会を開放しました。
地方の確立された製薬産業、強いヘルスケアのインフラおよび費用効果が大きいAutoimmuneの処置のための上昇の要求はbiosimilarsの増加の採用を支えます。 規制当局によるバイオシミラーの承認を合理化するための取り組みは、市場拡大を加速しています。
ヨーロッパHumiraバイオシミラー市場分析とトレンド
ヨーロッパは、バイオシミラーの採用の先駆者として、2025年のグローバル市場シェアの約30.7%を占めています。 明確な規制経路と支持政策の領域の初期の確立は、複数の承認され、Humiraバイオシミラーを立ち上げた競争力のある市場風景を育てています。
欧州諸国は、医療費の封入イニシアティブと成長する医師の受入によって駆動される高度化したバイオシミラーの取入口から恩恵を受けています。 ドイツ、英国、フランスは地域市場をリードし、強力な医薬品イノベーションと堅牢な医療システムを反映しています。
アジアパシフィックフミラバイオシミラー 市場分析とトレンド
アジアパシフィックは、2025年に約16.8%のシェアを占めるヒマラバイオシミラー市場において大きな成長を遂げています。 日本、韓国、オーストラリアなどの国々は、バイオシミラーの浸透を増加させ、自己免疫疾患の普及と手頃な価格の治療オプションのプレスの必要性によって推進されています。
規制環境や市場アクセスが地域に変化する一方で、承認プロセスの継続的な改善と、ヘルスケアインフラのサポートの拡大が進んでいます。 アジアパシフィックの新興市場も、バイオシミラーの採用の可能性を提示します。
Humira Biosimilar Marketのドミネーション国
アメリカ合衆国
米国は、高い医療費の運転、患者の意識の向上、および特許の暴露後にバイオシミラーの受諾を拡大する北アメリカで最大の市場です。 米国規制枠組みは、バイオシミラー市場参入を容易にするために進化しています。
カナダ
カナダのバイオシミラー市場は、費用対効果の高い医療を促進し、バイオシミラー療法へのアクセスを増やす政府の取り組みから恩恵を受けています。
ドイツ
ドイツは、初期のバイオシミラーの採用、好ましい償還方針、および強い製薬産業によって支えられるヨーロッパのヒマラのバイオシミラーの市場を、導きます。
イギリス
U.K.はNHSの費用節約プログラムおよび進歩的な調整の指導によって運転される急速な生物模倣のuptakeを表わします。
フランス
フランスは、医療改革によるバイオシミラー浸透を拡充し、患者様のアクセスを増加させることで、欧州市場を維持しています。
ジャパンジャパン
日本は医薬品市場を拡大し、栄養規制経路にもかかわらず、フミラバイオシミラーセグメントにおける自己免疫疾患前駆的成長を増加させました。
韓国
韓国のバイオシミラー市場は、政府の支援、ヘルスケア支出の増加、規制枠の改善のために成長しています。
マーケットレポートスコープ
Humiraバイオシミラー マーケットレポートカバレッジ
| レポートカバレッジ | ニュース | ||
|---|---|---|---|
| 基礎年: | 2024年(2024年) | 2025年の市場規模: | 1 成人 2 成人 3 成人 4 成人 5 成人 6 成人 7 成人 8 成人 9 成人 10 成人 |
| 履歴データ: | 2020年~2024年 | 予測期間: | 2025 へ 2032 |
| 予測期間 2025〜2032 CAGR: | 25.9% | 2032年 価値の投射: | 米ドル 7,724.0 Mn |
| 覆われる幾何学: |
| ||
| カバーされる区分: |
| ||
| 対象会社: | Amgen Inc.、Samsung Bioepis Co., Ltd.、Sandoz International GmbH(Novartis AG)、Mylan N.V.、Boehringer Ingelheim International GmbH、Pfizer Inc.、Fredsenius Kabi AG、Coherus BioSciences、Inc.、Biogen Inc.、AbbVie Inc.、Celltrion Inc.、Rani Therapeutics Holdings、Inc.、Teva Pharmaceutical Industries Ltd、Merck & Cove、Inc.、Inc.、AbbVia、AbbVia、AbbVie Inc.、AbbVia、AbbVia、AbbVia、Co.、Co.、AbbVia、AbbValtech、A、A、Ca、Ca、Ca、Ca、Ca、Ca、S、S、S、S、S、S、S、S、S、S、S、S、S、S、S、S、S、S、S、S、S、S、S、S、S、S、S、S、S、S、S、S、S | ||
| 成長の運転者: |
| ||
| 拘束と挑戦: |
| ||
75 以上のパラメータに基づいて検証されたマクロとミクロを発見: レポートにすぐにアクセス
グローバルヒマラバイオシミラー市場ドライバー
- 特許審査
ユーラを保護する特許の普及は、バイオシミラーのエントリのための方法を舗装しました。 特許が期限切れになったら、他の製薬会社が開発し、市場の競争を作成するユーモアのバイオシミラー版を販売することができます。
- コスト削減
Biosimilarsは、参照の生物学的薬へのより費用対効果の高い代替手段を提供します。 手頃な価格のヘルスケアに対する需要の増加に伴い、バイオシミラーは、患者、医療システム、および賃金の治療コストを削減する機会を提供します。 この費用節約の可能性は、ユーラバイオシミラーの採用のための重要なドライバです。 例えば、2023年10月26日、バイオ医薬品会社Celltrion USA, Inc.は、FDA承認バイオシミラー、YUFLYMA(adalimumab-aaty)を発表し、CarePartners Specialty Pharmacy Cost Saves Programに追加しました。
YUFLYMAは、Humira(adalimumab)バイオシミラーの高濃度(100mg / mL)およびクエン酸塩フリー処方です。 CarePartnersとその戦略的パートナーは、YUFLYMAを最低純コストの高濃度Humira(adalimumab)バイオシミラーとして10万人以上のプランメンバーに提供および配布します。
- 自己免疫疾患の早期増加
関節リウマチ、乾癬、およびクローン病などの自己免疫疾患は、世界的な上昇しています。 これらの条件の増殖の優先順位は、自己免疫疾患のための実証済みの治療法であるユーラのバイオシミラーを含む効果的でアクセス可能な治療の需要を促進します。
- 好ましい規制環境
様々な地域の規制機関は、バイオシミラーの承認と市場アクセスのためのガイドラインと経路を確立しました。 これらのフレームワークは明確性を提供し、ユーラバイオシミラーの開発、評価、および商品化を促進します。 好ましい規制環境は、製薬企業がバイオシミラーの開発に投資することを奨励します。
グローバルヒマラバイオシミラー市場機会
- 治療へのアクセスの増加
ユーミラバイオシミラーの可用性は、自己免疫疾患の患者のための治療へのアクセスを向上させる機会を提供しています。 Biosimilarsは、より手頃な価格の代替法を提供して、より広範な人口が効果的な治療法から恩恵を受けることを可能にします。
- 市場拡大と競争力
ユーミラバイオシミラーの導入により、市場における競争を創出し、イノベーションとコスト最適化を推進しています。 この競争は、製薬会社がバイオシミラーを開発し、発売することを奨励し、より競争力のある風景につながります。 また、患者様の多様な治療オプションの市場成長と発展を促進します。
- 高められた処置の選択
ユーミラバイオシミラーの可用性は、医師や患者のための治療選択肢の範囲を拡大します。 医師は、患者のニーズ、価格設定、臨床証拠などの要因に基づいて、複数のバイオシミラーオプションから選択できます。 患者は、特定の条件と好みに合わせて調整される治療のより広い選択から利益を得ることができます。
- グローバル市場拡大
ユーモアラバイオシミラー市場は、グローバル展開のための機会を提示します。 バイオシミラーの規制経路とガイドラインは、世界中で進化し、改善を続けています。製薬会社は、さまざまな地域で承認を求めることができます。これにより、新しい市場に参入し、より大きな患者集団に到達します。
グローバルヒマラバイオシミラー市場動向
- 規制の承認と市場参入
規制機関は、ユーミラを含むバイオシミラーの承認と市場参入のための経路とガイドラインを確立しました。 ユーラバイオシミラーの規制当局の承認の数が増加し、市場可用性と採用を拡大することができます。
- 市場拡大と地域の変動
ユーモアラバイオシミラー市場は、様々な地域でバイオシミラーが利用できるようになり、世界中で拡大しています。 ヨーロッパはバイオシミラーの採用の最前線にありました、承認されたユーラバイオシミラーの比較的高い数で。 しかし、北米、アジアパシフィック、中南米を含む他の地域も、ユーラバイオシミラーの参入と成長を目撃しています。
- 医師と患者の受け入れ
医師は、バイオシミラー、バイオシミラーの受け入れや採用を処方することで、より多くの経験と自信を得るため、増加しています。 バイオシミラーの患者受け入れも成長しています, 肯定的な臨床結果などの要因によって駆動, コスト削減, 治療オプションへのアクセスを改善.
- コラボレーションとパートナーシップ
製薬会社、ヘルスケアプロバイダー、およびペイアー間の協業パートナーシップが、ユーミラバイオシミラーの開発、市場アクセス、および採用を推進しています。 そのようなコラボレーションは、患者のアクセス、教育、およびバイオシミラーに関する意識の向上、ならびに潜在的な障壁を彼らの取組に取り組むことを目指しています。
アナリスト視点
- Humira Biosimilar市場は、主にキー領域にわたって有利な特許の普及によって駆動され、グローバルバイオロジカルランドスケープの変革シフトを指しています。 主要な市場ドライバーは、バイオシミラーが元のHumiraに匹敵する治療効果を維持しながら、実質的なコスト節約を提供するため、製薬支出を抑制するヘルスケア部門の緊急の必要性です。 関節リウマチ、クローン病、乾癬などの自己免疫障害の上昇可能性は、アドリママブの治療の需要を拡大し続けています。
- それにもかかわらず、市場は注目すべき課題に直面しています。 複雑な規制経路では、バイオシミラリティを実証するために広範囲の臨床試験が必要ですが、医師は患者を確立したバイオロジカルを切り替えることを躊躇します。 さらに、特許訴訟戦略とモノクローナル抗体の複合体を製造する新たな参入者に障壁をポーズします。
- これらの制約にもかかわらず, 重要な機会は、バイオシミラーの開発者と医療従事者の間で戦略的なコラボレーションを通じて発生し、処方オプションを拡大することを目指しています. 医療従事者および支援政府の政策におけるバイオシミラー受入の増加により、成長の有利な条件が生まれます。
- 地域的に, ヨーロッパは、以前の特許の有効期限と堅牢な規制枠組みのためにリードします. 北米は急速に成長する市場であり、最近の特許崖は、複数のバイオシミラー打ち上げと激しい競争をトリガーします。 アジア・パシフィック地域は、規制システムが成熟し、医療アクセスのイニシアティブが手頃な価格のバイオロジカルセラピーを優先する可能性を示す。
最近の開発
- アリダ(adalimumab-atto): ABRILADAは、リウマチド関節炎、ジュベニル性関節炎、乾性関節炎、膿疱性脊髄炎、成人クローン病、潰瘍性関節炎およびプラーク乾癬の特定の患者の治療のためにユーラにクエン酸塩フリーバイオシミラーです。 2023年10月5日、米国FDAはアブリラダ(adalimumab-afzb)への交換性を付与し、指定を受ける2番目のアドリムマブバイオシミラー。
- ユシムリ(adalimumab-aqvh):ユーシモーリ(adalimumab-aqvh)、ユーミラ(adalimumab)の生物類似体は、腫瘍の壊死因子(「TNF」)のブロッカーで、リウマチの徴候と症状を減らすために示され、イディオパシー性関節炎、乾性関節炎、および膿疱性脊椎炎、および結腸炎の治療、および肺炎および肺炎および肺炎および肺炎および肺炎および肺炎および肺炎の肺炎および肺炎および肺炎。 7月 03, 2023, Coherus BioSciences, Inc., 商業段階のバイオ医薬品会社, YUSIMRY (adalimumab-aqvh) が米国での商用販売のために利用可能であることを発表しました. 米国のリストの価格で US $ 995 2 40 mg/0.8 mL オートインジェクタのためのカートンあたり, 以上の割引を表す85%のユーモアラ(adalimumab)に、現在2本のペンのカートンごとのUS $ 6,922で販売されています。
- AMJEVITA(adalimumab-atto): AMJEVITAは、抗TNF-αモノクローナル抗体であるHumira(adalimumab)にバイオシミラーです。 AMJEVITAの有効成分は、ユーミラと同じアミノ酸シーケンスを持つ抗TNF-αモノクローナル抗体です。 2023年1月31日、米国多国籍バイオ医薬品会社であるAmgenは、アメリカでバイオシミラーであるAMJEVITA(adalimumab-atto)を発表しました。アメリカで利用可能です。
買収とパートナーシップ
- 2023年7月24日、世界規模のバイオテクノロジー企業であるジェネリック医薬品および革新的な医薬品のグローバルリーダーであるTeva Pharmaceuticals, Inc.は、世界中の患者を対象としたバイオシミラー薬の開発・製造を専門とするグローバルバイオテクノロジー企業であり、既存の戦略的パートナーシップ協定の拡大に合意したことを発表しました。 Teva Pharmaceuticals, Inc. はまた、Alvotech が発行するサブ座標変換可能な債券を取得します。 パートナーは、ユーモア(アダリムマブ)の交換可能な高濃度バイオシミラー候補であるAVT02の米国における保留承認に関する問題に密接に取り組んでいます。 既存の戦略的パートナーシップ協定には、米国食品医薬品局(FDA)の承認を保留しているStelara(ustekinumab)のための提案されたバイオシミラーであるAVT04である他の4つのバイオシミラー候補も含まれています。
- 6月05日、2023日、Rani Therapeutics バイオ医薬品および医薬品の経口配送に焦点を当てた臨床段階のバイオ医薬品会社である株式会社ホールディングスは、同社は、経口投与されたアドリママブバイオシミラーであるRT-105の開発のための合意に入ったバイオ医薬品会社であるCelltrion, Inc.とパートナーシップを拡大したことを発表しました。 Raniの治療薬 ホールディングス、株式会社セルトリオンとの最初のパートナーシップを締結しました。RT-111の開発、経口投与されたユーテキンマブバイオシミラーは、2023年1月に発表されました。 新しいライセンスと供給契約の条項の下で、CelltrionはRani Therapeutics Holdings, Inc.、RT-105に必要なadalimumabバイオシミラー薬物質(CT-P17)に独占的に供給します。 Rani Therapeutics Holdings, Inc.は、RT-105の開発および商用化においてCT-P17を使用する独占ライセンスを付与し、Celltrionは、第1フェーズ1研究後にRT-105に世界的権利を獲得するための最初の交渉権を付与しました。
- 6月01日、2023日、マーク・キューバン コストプラス医薬品 当社は、グローバルバイオシミラー会社であるコヘルスバイオサイエンス株式会社と、マーク・キューバ・コスト・プラス・ドラッグ・カンパニーの顧客であるユーシムリー(adalimumab-aqvh)、HUMIRA(adalimumab注射)のバイオシミラーであるマーク・キューバ・コスト・プラス・ドラッグ・カンパニー(adalimumab-aqvh)を提供する予定です。 マーク・キューバン コストプラス医薬品 当社は、お客様に対し、US $ 569.27 の料金で YUSIMRY をお客様に提供する予定です。
市場区分
- 製品タイプ別
- Biosimilar Humira(アダリママブ)
- 交換可能なバイオシミラーHumira
- インディケーション
- Rheumatoid関節炎
- 乾癬
- クローン病
- 潰瘍性関節炎
- 脊髄膜炎
- ジュヴェニル・イディオパシー 関節炎
- その他のAutoimmune条件
- 患者の年齢によって
- 大人の患者
- 小児患者
- 胃の患者
- 流通チャネル
- 病院薬局
- 小売薬局
- オンライン薬局
- 地域別
- 北アメリカ
- アメリカ
- カナダ
- ラテンアメリカ
- ブラジル
- アルゼンチン
- メキシコ
- ラテンアメリカの残り
- ヨーロッパ
- ドイツ
- アメリカ
- スペイン
- フランス
- イタリア
- ロシア
- ヨーロッパの残り
- アジアパシフィック
- 中国・中国
- インド
- ジャパンジャパン
- オーストラリア
- 韓国
- アセアン
- アジアパシフィック
- 中東
- GCCについて 国土交通
- イスラエル
- 中東の残り
- アフリカ
- 南アフリカ
- 北アフリカ
- 中央アフリカ
- 北アメリカ
- グローバルフミラバイオシミラー市場トップ企業
- アミューゲン
- サムスンバイオエピス株式会社
- Sandoz International, オーストラリア ノヴァラティスAG
- マイランN.V.
- ボヘリンガー インゲルハイム インターナショナル GmbH
- 株式会社Pfizer
- FreseniusのKabiのAG
- Coherus バイオサイエンス株式会社
- バイオジェン株式会社
- 株式会社AbbVie
- セルトリオン株式会社
- ラニ・セラピューティクス・ホールディングス株式会社
- Tevaの薬剤 株式会社インダストリーズ
- マーク&株式会社
- バイアトリス株式会社
- アルボテック
ソース
第一次研究インタビュー
- 製薬産業エグゼクティブ
- 規制業務スペシャリスト
- ヘルスケアプロバイダーおよび医師
- バイオシミラーメーカー
- その他
データベース
- アメリカ オレンジブックデータベース
- 電子メール 欧州パブリックアセスメントレポート(EPAR)
- WHOグローバルヘルス天文台
- IQVIA ヘルスケアデータベース
- その他
雑誌
- バイオファーマ ダイビング
- 医薬品事業部
- バイオワールドインテリジェンス
- バイオシミラー開発
- その他
ジャーナル
- 自然バイオテクノロジー
- バイオドラッグジャーナル
- 医薬品科学ジャーナル
- その他
新聞
- ウォールストリートジャーナル
- 金融タイムズ
- ロイター健康ニュース
- ブルームバーグ医薬品 ニュース
- その他
協会について
- アクセシブル医薬品協会(AAM)
- 欧州医薬品庁(EMA)
- バイオシミラーズ協議会
- 国際ジェネリック医薬品協会(IGBA)
- その他
パブリックドメインソース
- アメリカ 医薬品承認とデータベース
- 臨床試験レジストリ(ClinicalTrials.gov)
- 特許・商標事務所の記録
- SECファイリングレポート
- その他
独自の要素
- ログイン データ分析ツール
- プロモーション CMI 過去8年間の情報の登録
*定義:Humiraバイオシミラーは、ユーモアラの特許の満了後に開発および承認されたバイオロジック薬ユーラ(adalimumab)の非常に類似したバージョンです。 これらのバイオシミラーは、ユーモアに同等の有効性、安全性、品質を持つように設計されており、リューマチノイド関節炎、乾癬、およびクローン病などの自己免疫疾患患者のためのより手頃な価格の治療オプションを提供します。
著者について
Nikhilesh Ravindra Patel は、8 年以上のコンサルティング経験を持つシニア コンサルタントです。市場予測、市場インサイト、トレンドと機会の特定に優れています。市場動向に対する深い理解と成長分野を正確に特定する能力により、情報に基づいたビジネス上の意思決定をクライアントに導く上で、彼は非常に貴重な存在となっています。レポートを通じて、市場情報、ビジネス情報、競合情報サービスを提供する上で重要な役割を果たしています。
独占トレンドレポートで戦略を変革:
よくある質問